Adalimumab (HALIMATOZ®) - Biosimilaire
Attention :
Le 18 décembre 2020, la Commission européenne a retiré l'autorisation de mise sur le marché d'HALIMATOZ (adalimumab) dans l'Union européenne (UE).
Structure : AcM humain, IgG1k
Code ATC : L04AB04 (Antinéoplasiques et immunomodulateurs L04 Immunosuppresseurs L04A Immunosuppresseurs L04AB Inhibiteurs du facteur de nécrose tumorale alpha (TNF-alpha) L04AB04 Adalimumab)
Nomenclature Ge : IgG1κ G1e0
Cible: TNF (tumor necrosis factor) soluble et membranaire
Mode d'administration : SC
Date de la première AMM : EMA juillet 2018
Laboratoires : Sandoz GmbH
Indications : polyarthrite rhumatoïde, arthrite juvénile idiopathique, spondylarthrite axiale, rhumatisme psoriasique, psoriasis, hidrosadénite suppurée, uvéite
Prix indicatif : xxx
Usage : prescription initiale hospitalière annuelle
Posologies :
Pour la polyarthrite, la spondylarthrite ankylosante, le rhumatisme psoriasique et l'arthrite juvénile idiopathique 40 mg/2 semaines.
Pour le psoriasis et l'uvéite 80 mg d'emblée puis 40 mg/2 semaines dès la semaine 1.
Pour l'hidrosadénite suppurée (HS) une dose initiale de 160 mg au Jour 1 (administrée sous forme de 4 injections de 40 mg sur un jour ou de 2 injections de 40 mg par jour pendant deux jours consécutifs), suivie d'une dose de 80 mg deux semaines après au Jour 15 (administrée sous forme de 2 injections de 40 mg sur un jour). Deux semaines plus tard (Jour 29), poursuivre avec une dose de 40 mg chaque semaine ou de 80 mg toutes les deux semaines (administrés sous forme de deux injections de 40 mg par jour).
Mécanisme d'action :
L'adalimumab bloque le TNF trimérique soluble et membranaire, ce qui empêche l'interaction avec les récepteurs p55 (TNFR1) et p75 (TNFR2) situés à la surface cellulaire, qui aurait permis l'activation de la voie NF-kB avec synthèse de cytokines pro-inflammatoires. La cascade inflammatoire est ainsi bloquée : diminution de l'expression de molécules d'adhésion diminuant ainsi le processus de diapédèse, et de recrutements de macrophages, lymphocytes et neutrophiles.
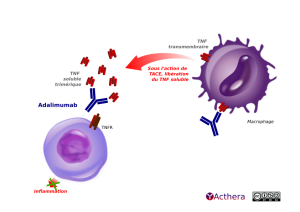
En haut, à droite, un macrophage porteur de deux TNF transmembranaires. L’un des TNF est à gauche sur la membrane. Un second TNF transmembranaire se trouve en bas de la membrane. Il est en contact avec un anticorps adalimumab (anticorps I g G 1 humain) qui bloque son action.
Plus bas à gauche, un lymphocyte T exprime un récepteur du TNF (légendé TNFR).
Une flèche courbe part du TNF, présent sur la gauche de la membrane du macrophage, elle pointe vers les TNF solubles trimériques situés au-dessus du lymphocyte T. Elle porte la légende : « Sous l'action de TACE, libération du TNF soluble » (TACE est l'enzyme de conversion du TNF alpha).
L'adalimumab se lie aux TNF solubles trimériques qui essaient de se connecter au TNFR présent sur la membrane du lymphocyte T. Une flèche barrée d’une croix hors du lymphocyte T, pointe sur le mot « Inflammation », attestant la réduction de l’inflammation par l’adalimumab.
Effets indésirables les plus fréquents :
Les effets secondaires les plus fréquents (qui peuvent toucher plus d'une personne sur 10) sont les infections (y compris dans le nez, la gorge et les sinus), les réactions au site d'injection (rougeur, démangeaison, saignement, douleur ou gonflement), les maux de tête et les douleurs musculaires et osseuses.
D'autres effets secondaires graves et rares (pouvant toucher jusqu'à 1 personne sur 1 000) incluent l'incapacité de la moelle osseuse à produire des cellules sanguines, des lésions nerveuses causées par la dégradation de l'enveloppe des fibres nerveuses, le lupus et les affections apparentées au lupus, et le syndrome de Stevens-Johnson.
Contre-indications : Tuberculose active, infections graves (septicémie, infections opportunistes), insuffisance cardiaque
Utilisation chez la femme enceinte : Le CRAT considère qu’il n’y a pas d’association établie entre un effet malformatif particulier et l’exposition concernée (passage des Ig1 transplacentaires après la 14e SA donc après la fin de l'organogénèse). L'adalimumab passe le placenta : à la naissance, les concentrations maternelles néonatales sont supérieures aux concentrations plasmatiques maternelles. Parmi plus de 3000 patientes exposées en 2e partie de grossesse à un anti-TNF alpha (infliximab et adalimumab), dont 1500 au 3e trimestre de grossesse, aucun effet attribuable au traitement n'est retenu (prématurité, infections...) chez les enfants suivis jusque l'âge de 5 ans. Donc on conseille une consultation pré-conceptionnelle pour faire le point sur la pathologie. L'adalimumab peut être poursuivi pendant la grossesse en tenant compte du risque de l'immunosuppression du traitement. La concentration de l'adalimumab dans le lait est très faible, voire indétectable, de même que dans le sang des enfants ayant été allaités par une mère traitée.
Principales références :
- Sandborn WJ et al., Adalimumab induces and maintains clinical remission in patients with moderate-to-severe ulcerative colitis, 2012 , Gastroenterology ; 142:257-65
- BeukelmanT et al., American College of Rheumatology recommendations for the treatment of juvenile idiopathic arthritis, 2011, Arthritis Care Res ; 63:465-82
Liens
- fiche médicament du adalimumab sur le site du GETAID
- Lien vers Human medicine European public assessment report (EPAR)
Remarque :
Dernière mise à jour : août 2022
Relecture par : Mathilde GLAZIOU