Elotuzumab (EMPLICITI®)
Structure : AcM humanisé, IgG1
Code ATC : L01FX08
Nomenclature Ge : IgG1κ G1e0
Cible: protéine SLAMF7 (Signaling lymphocyte activation molecule family member 7)
Mode d'administration : IV
Date de la première AMM : EMA 2016 / FDA 2015
Laboratoires : Bristol-Meyers Squibb/ AbbVie
Indications : en combinaison au lénalidomide et la dexaméthasone dans le traitement du myélome multiple ayant déjà reçu au moins un traitement
Prix indicatif :
Usage : réservé à l'usage hospitalier
Posologies : 10 mg/kg par semaine en combinaison avec la dexaméthasone 28 mg en VO, pendant 4 semaines (=2 cycles). Au cours de ces 2 cycles, la dose recommandée de lénalidomide est de 25 mg/j pendant 21 jours (VO).
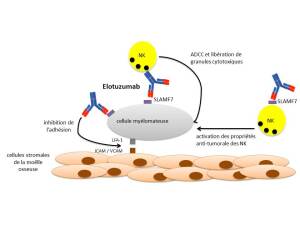
Mécanisme d'action :
Elotuzumab possède deux mécanismes d'action complémentaires. Tout d'abord en se fixant directement sur les cellules du myélome multiple qui surexpriment SLAMF7 et en induisant un mécanisme de cytotoxicité médiée par les anticorps (ADCC). Cette interaction diminue également l'adhésion des cellules myélomateuses aux cellules stromales de la moëlle osseuse, favorisant ainsi leur apoptose. Il peut également se lier sur le SLAMF7 exprimé à la surface des cellules NK. Cette interaction a pour conséquence d'activer les cellules NK et de stimuler leur capacité anti-tumorale.
Effets indésirables les plus fréquents: zona, pneumonies, infections des voies respiratoires supérieures, lymphopénie, neuropathies périphériques
Contre-indications : hypersensibilité au médicament
Principales références :
- Lonia S et al., Elotuzumab Therapy for Relapsed or Refractory Multiple Myeloma, N Engl J Med, 2015, 13;373(7):621-31 ; Dimopoulos M et al., ELOQUENt-2 update : a phase III, randomized, open-label study of elotuzumab in combination with lenalidomide/dexamethasone in patients with relapsed/refractory multiple myeloma - 3 year safety and efficacy follow-up. Blood, 126:28
- Lien vers Human medicine European public assessment report (EPAR)