Risankizumab (SKYRIZI®)
Structure : AcM humanisé IgG1
Code ATC : L04AC18
Nomenclature Ge : IgG1κ G1e10
Cible : IL-23 (sous-unité p19)
Mode de production : Produit par des cellules ovariennes de hamster chinois par la technique de l'ADN recombinant
Forme galénique :
- SKYRIZI 150 mg S inj seringue préremplie Ser/1ml
- SKYRIZI 150 mg Sol inj stylo prérempli Stylo/1ml
- SKYRIZI 75 mg, solution injectable
- SKYRIZI 90 mg/ml S inj en seringue préremplie Ser [ATUn]
- SKYRIZI 90 mg/ml S perf en flacon Fl [ATUn]
Mode d'administration : SC
Date de la première AMM : EMA avril 2019 / FDA 2019
Laboratoires : AbbVie
Indications : traitement du psoriasis en plaques modéré à sévère chez l'adulte qui nécessite un traitement systémique
Prix indicatif : 2 743,12 euros pour la boîte de 2 seringues préremplies (2021)
Usage : Prescription initiale hospitalière annuelle. Prescription initiale et renouvellement réservés aux spécialistes en dermatologie ou en médecine interne
Posologies :
Skyrizi 150 mg, solution injectable en stylo prérempli et seringue préremplie
La dose recommandée est de 150 mg administrée en injection sous-cutanée à la semaine 0, à la semaine 4, puis toutes les 12 semaines.
Skyrizi 75 mg, solution injectable en seringue préremplie
La dose recommandée est de 150 mg (soit deux injections de 75 mg) administrée en injection sous-cutanée à la semaine 0, à la semaine 4, puis toutes les 12 semaines.
Une interruption du traitement devra être envisagée chez les patients n'ayant pas répondu après 16 semaines de traitement. Chez certains patients ayant obtenu une réponse initiale partielle, une amélioration ultérieure peut être observée en poursuivant le traitement au-delà de 16 semaines.
Mécanisme d'action :
Le risankizumab se lie sélectivement et avec une forte affinité à la sous-unité p19 de la cytokine humaine interleukine-23 (IL-23) sans se lier à l'IL-12, ce qui inhibe l'interaction avec le complexe récepteur de l'IL-23. L'IL-23 est une cytokine impliquée dans les réponses immunitaires et inflammatoires. En empêchant la liaison de l'IL-23 à son récepteur, le risankizumab inhibe la voie de signalisation cellulaire de l'IL-23 et la libération des cytokines pro-inflammatoires
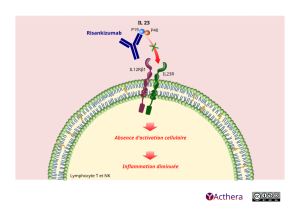
Au centre de l’illustration, une cellule NK ou Lymphocyte T. Au sommet de sa membrane deux récepteurs se font face : à gauche un « IL 12R bêta1 » et un « IL 23R ».
Au dessus de la cellule se trouve l’IL 23. Il se compose de deux sous-unités – deux sphères qui se touchent. À gauche P 19 à droite P 40.
L’anticorps monoclonal risankizumab se lie à la sous-unité P19 de l’interleukine 23 (IL 23). L’IL 23 régule, la différentiation, l’expansion et la survie de certaines catégories de cellules dont le lymphocyte-T et certaines sous-populations de cellules de l’immunité innée : IL 17A, IL 17F et IL 22 impliquées dans l’inflammation. Une flèche rouge barrée pointe depuis les sous-unités d’IL 23 sur le récepteur IL 23R, signale que risankizumab empêche l’IL 23 de se lier à l’IL 23 R.
Dans la cellule sous les récepteurs IL 12R bêta1 et IL 23R une flèche pointe en bas sur le texte « Absence d’activation cellulaire ». Sous ce texte une autre flèche désigne plus bas le texte « Inflammation diminuée ». L’action de risankizumab perturbe le signal et provoque ainsi la baisse de l’inflammation. Le risankizumab permet une régulation de la production des cytokines IL 23.
Le risankizumab exerce ses effets cliniques sur le psoriasis en plaques et sur le rhumatisme psoriasique par le blocage de la voie cytokinique de l'IL 23.
• Effets indésirables les plus fréquents: infections des voies respiratoires supérieures
• Contre-indications : Hypersensibilités, infections actives cliniquement importantes (par exemple : tuberculose active)
• Principales références :
Liens :
- Human medicine European public assessment report (EPAR)
- Avis de la HAS sur SKYRIZI®
- Base de données publique des médicaments
- ANSM
- Meddispar
- Vidal
- Centre de référence sur les agents tératogènes (CRAT)
- IMGT/mAb-DB
- Vidéos d'aide à l'administration du .... en stylo et en seringue (français)
- Lien vers
-
- Lien vers la fiche info de la base de données publique des médicaments
- IMGT
- HeTOP
Remarque :
Dernière mise à jour : Novembre 2021
Relecture par : Dr Emmanuel Hermann