Dupilumab (DUPIXENT®)
Code ATC : D11AH05
Structure : AcM humain, IgG4
Nomenclature Ge : IgG4κ G4e1
Cible: IL-4Ra, chaine alpha commune au récepteurs à l'IL-4 et l'IL-13
Mode d'administration : SC
Forme galénique : Solution injectable en seringue ou en stylo prérempli de 300 mg ou de 200 mg.
Date de la première AMM : EMA septembre 2017 / FDA mars 2017
Laboratoires : sanofi-aventis groupe
Indications :
- Modérée à sévère chez les adultes et adolescents de plus de 12 ans nécessitant un traitement systémique
- Sévère chez les enfants âgés de 6 mois à 11 ans
Asthme :
- En traitement de fond additionnel de l'asthme sévère associé à une inflammation de type 2, caractérisée par des éosinophiles sanguins élevés et/ou une fraction de monoxyde d'azote expiré (FeNO) élevée, chez les adultes et les adolescents de 6 ans et plus qui sont insuffisamment contrôlés par des corticostéroïdes inhalés à dose élevée associés à un autre traitement de fond de l'asthme.
Rhinosinusite chronique avec polypose nasale :
- Pour les adultes, en traitement additionnel aux corticostéroïdes par voie nasale chez les adultes présentant une polypose naso-sinusienne sévère insuffisamment contrôlés par des corticostéroïdes systémiques et/ou la chirurgie.
Prurigo nodulaire :
- Modéré à sévère de l’adulte qui nécessite un traitement systémique
Oesophagite à éosinophile :
- Chez l’adulte et l’adolescent âgé de 12 ans et plus et pesant au moins 40 kg, en cas d’échec, de contre-indication ou d’intolérance aux traitements médicamenteux conventionnels
Bronchopneumopathie Chronique Obstructive (BPCO) :
- Chez les adultes en traitement de fond additionnel de la BPCO caractérisée par un taux élevé d'éosinophiles sanguins, non contrôlée par l'association corticostéroïdes inhalés (CSI), béta-2-agoniste à longue durée d'action (LABA) et antagoniste muscarinique de longue durée d'action (LAMA) ou par l'association LABA/LAMA seule si les CSI ne sont pas adaptés
Prix indicatif TTC (2025) : 608.33 € pour une seringue de 300 mg ou de 200 mg (658,87 € en 2023).
Usage : Médicament soumis à prescription initiale hospitalière (PIH) annuelle. Prescription initiale et renouvellement réservés aux spécialistes en dermatologie, en pneumologie, en pédiatrie, en médecine interne, oto-rhino-laryngologie ou en allergologie.
Posologies :
Dermatite atopique :
Adultes : une dose initiale de 600 mg (deux injections de 300 mg), suivie de 300 mg administrés toutes les deux semaines.
Adolescents (âgés de 12 à 17 ans) :
- pour les adolescents > 60 kg ou plus : dose initiale de 600 mg (deux injections de 300 mg), suivie de 300 mg administrés toutes les deux semaines
- pour les adolescents < 60 kg : dose initiale de 400 mg (deux injections de 200 mg), suivie de 200 mg administrés toutes les deux semaines
Enfants âgés de 6 à 11 ans :
- pour les enfants > 60 kg : dose initiale de 600 mg (deux injections de 300 mg), suivie de 300 mg administrés toutes les deux semaines
- pour les enfants de 15 kg à < 60 kg une dose de 300 mg à J1, puis 300 mg à J15, suivie de 300 mg toutes les 4 semaines
Enfants âgés de 6 mois à 5 ans :
- pour les enfants de >15 kg à 30 kg : dose initiale de 300 mg suivie d'une injection de 300 mg toutes les 4 semaines.
- pour les enfants de 5 à 15 kg : dose initiale de 200 mg suivie d'une injection de 200 mg toutes les 4 semaines
Asthme :
Chez l'adulte et l'adolescent (âgé de 12 ans et plus) :
- 600 mg puis 300 mg toutes les 2 semaines pour l’asthme sévère traité par des corticostéroïdes oraux ou pour l’asthme sévère associé à une dermatite atopique modérée à sévère ou associé à une polypose naso-sinusienne sévère chez l’adulte
- 400 mg, puis 200 mg toutes les deux semaines pour les autres situations
Chez l'enfant entre 6 et 11 ans : la posologie dépend du poids
- > ou = 60 kg : 200 mg toutes les 2 semaines
- 30-60kg : 200 mg toutes les 2 semaines ou 300 mg toutes les 4 semaines
- 15-30 kg : 100 mg toutes les 2 semaines ou 300 mg toutes les 4 semaines
Rhinosinusite chronique avec polypose nasale : Chez l’adulte, dose initiale de 300 mg suivie d’une dose de 300 mg administrée toutes les deux semaines.
Prurigo nodulaire : Chez l’adulte, dose initiale de 600 mg (deux injections de 300 mg), suivie d’une dose de 300 mg administrée toutes les deux semaines
Oesophagite à éosinophile : Chez l’adulte et l’adolescent âgé de 12 ans et plus, 300 mg administrés toutes les semaines
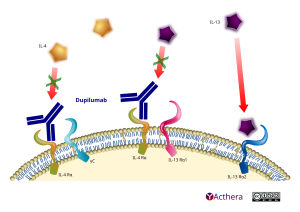
Mécanisme d'action :
Le dupilumab inhibe la signalisation de l'interleukine-4 (IL-4) et l'interleukine-13 (IL-13), des cytokines majeures de type 2 (notamment Th2) impliquées dans la dermatite atopique. Le dupilumab inhibe la signalisation de l'IL-4 via le récepteur de type I (IL-4Rα/γc), et la signalisation à la fois de l'IL-4 et l'IL-13 via le récepteur de type II (IL-4Rα/IL-13Rα). Le dupilumab peut agir sur l’inhibition de la différenciation des cellules Th2, la transformation des cellules Treg en cellules ex-Treg dans le contexte d'une inflammation allergique et la production d'IgE par les cellules B, induite par l'IL-4. Il peut également inhiber l'induction d'ILC2 via les éosinophiles et les basophiles.
Effets indésirables les plus fréquents: réactions au site d'injection, la conjonctivite, la blépharite, et l'herpès buccal. (se référer au RCP pour avoir la liste complète des effets indésirables).
Contre-indications : hypersensibilité au dupilumab ou à l'un des excipients.
Surveillance particulière : Les patients souffrant d'infections par les helminthe doivent être traités avant de commencer Dupixent. Ceux infectés en cours de traitement et qui ne répondent pas aux antihelminthiques doivent interrompre Dupixent jusqu'à la guérison de l'infection.
Principales références :
- Harb H, Chatila TA. Mechanisms of Dupilumab. Clin Exp Allergy. 2020 Jan;50(1):5-14. doi: 10.1111/cea.13491. Epub 2019 Sep 30. PMID: 31505066; PMCID: PMC6930967.
- Xiong XF, Zhu M, Wu HX, Fan LL, Cheng DY. Efficacy and safety of dupilumab for the treatment of uncontrolled asthma: a meta-analysis of randomized clinical trials. Respir Res. 2019 May 31;20(1):108. doi: 10.1186/s12931-019-1065-3. PMID: 31151443; PMCID: PMC6544936.
- Hoy SM. Dupilumab: A Review in Chronic Rhinosinusitis with Nasal Polyps. Drugs. 2020 May;80(7):711-717. doi: 10.1007/s40265-020-01298-9. PMID: 32240527.
- Agache I, Song Y, Posso M, Alonso-Coello P, Rocha C, Solà I, Beltran J, Akdis CA, Akdis M, Brockow K, Chivato T, Del Giacco S, Eiwegger T, Eyerich K, Giménez-Arnau A, Gutermuth J, Guttman-Yassky E, Maurer M, Ogg G, Ong PY, O'Mahony L, Schwarze J, Werfel T, Canelo-Aybar C, Palomares O, Jutel M. Efficacy and safety of dupilumab for moderate-to-severe atopic dermatitis: A systematic review for the EAACI biologicals guidelines. Allergy. 2021 Jan;76(1):45-58. doi: 10.1111/all.14510. Epub 2020 Oct 4. PMID: 32691892.
Liens :
- Human medicine European public assessment report (EPAR)
- Avis de la HAS sur Dupixent
- fiche info de la base de données publique des médicaments
- IMGT
- HeTOP
- CRAT
- Vidal
- Vidéos d'aide à l'administration du dupilumab en stylo et en seringue (français)
Note :
Création de la fiche : Pr C. Carnoy
Dernière mise à jour : Mars 2025
Relecture par : Mathilde GLAZIOU