Tixagevimab cilgavimab (EVUSHELD®)
Structure : Tixagevimab et cilgavimab sont deux anticorps monoclonaux recombinants humains IgG1kappa, avec des substitutions d’acides aminés dans les régions Fc, pour prolonger la demi-vie des anticorps et pour réduire leur fonction effectrice et le risque potentiel de renforcement de la maladie par les anticorps
Code ATC : J06BD03
Nomenclature Ge : IgG1κ G1e15
Mode de production : produits par la technique de l’ADN recombinant sur cellules d’ovaire de hamster chinois (CHO)
Forme galénique : Chaque boîte contient deux flacons :
Chaque flacon de tixagévimab contient 150 mg de tixagévimab dans 1,5 mL de solution (100 mg/mL).
Chaque flacon de cilgavimab contient 150 mg de cilgavimab dans 1,5 mL de solution (100 mg/mL).
Mode d'administration : IM
Date de la première AMM : FDA aout 2021 / EMA mars 2022
Laboratoires et lien vers xxx: AstraZeneca AB
Indications : indiqué en prophylaxie pré-exposition de la COVID-19 chez les adultes et les adolescents âgés de 12 ans et plus pesant au moins 40 kg
Prix indicatif (année) : XXX
Usage : xxx
Posologies :
La dose recommandée chez les adultes et les adolescents âgés de 12 ans et plus pesant au moins 40 kg est de 150 mg de tixagévimab et 150 mg de cilgavimab, administrés consécutivement sous forme de deux injections intramusculaires distinctes
Mécanisme d'action :
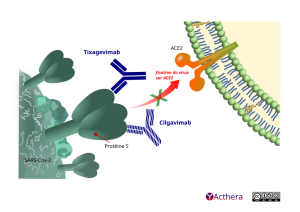
Le tixagévimab et le cilgavimab peuvent simultanément se lier à des régions non chevauchantes du domaine de liaison au récepteur (RBD) de la protéine spike du SARS-CoV-2. Le tixagévimab, le cilgavimab et leur association se lient à la protéine spike avec des constantes de dissociation d’équilibre KD de respectivement 2,76 pM, 13,0 pM et 13,7 pM, bloquant son interaction avec le récepteur ACE2 humain, entraînant un blocage de l’entrée du virus.
Effets indésirables les plus fréquents : (se référer au RCP pour avoir la liste complète des effets indésirables)
Contre-indications : Hypersensibilité aux substances actives ou à l’un des excipients
Principales références :
- Loo YM, McTamney PM, Arends RH, Abram ME, Aksyuk AA, Diallo S, Flores DJ, Kelly EJ, Ren K, Roque R, Rosenthal K, Streicher K, Tuffy KM, Bond NJ, Cornwell O, Bouquet J, Cheng LI, Dunyak J, Huang Y, Rosenbaum AI, Pilla Reddy V, Andersen H, Carnahan RH, Crowe JE Jr, Kuehne AI, Herbert AS, Dye JM, Bright H, Kallewaard NL, Pangalos MN, Esser MT. The SARS-CoV-2 monoclonal antibody combination, AZD7442, is protective in nonhuman primates and has an extended half-life in humans. Sci Transl Med. 2022 Mar 9;14(635):eabl8124. doi: 10.1126/scitranslmed.abl8124. Epub 2022 Mar 9. PMID: 35076282; PMCID: PMC8939769.
- Kotton CN. Belt and Suspenders: Vaccines and Tixagevimab/Cilgavimab for Prevention of COVID-19 in Immunocompromised Patients. Ann Intern Med. 2022 Apr 12:M22-1026. doi: 10.7326/M22-1026. Epub ahead of print. PMID: 35404669; PMCID: PMC9026000.
- Levin MJ, Ustianowski A, De Wit S, Launay O, Avila M, Templeton A, Yuan Y, Seegobin S, Ellery A, Levinson DJ, Ambery P, Arends RH, Beavon R, Dey K, Garbes P, Kelly EJ, Koh GCKW, Near KA, Padilla KW, Psachoulia K, Sharbaugh A, Streicher K, Pangalos MN, Esser MT; PROVENT Study Group. Intramuscular AZD7442 (Tixagevimab-Cilgavimab) for Prevention of Covid-19. N Engl J Med. 2022 Apr 20. doi: 10.1056/NEJMoa2116620. Epub ahead of print. PMID: 35443106.
- Corti D, Purcell LA, Snell G, Veesler D. Tackling COVID-19 with neutralizing monoclonal antibodies. Cell. 2021 Jun 10;184(12):3086-3108. doi: 10.1016/j.cell.2021.05.005. Epub 2021 May 26. Erratum in: Cell. 2021 Aug 19;184(17):4593-4595. PMID: 34087172; PMCID: PMC8152891.
Liens :
- Human medicine European public assessment report (EPAR)
- HAS
- Base de données publique des médicaments (pas disponible au 5 mai 2022)
- ANSM
- Meddispar (pas disponible au 5 mai 2022)
- Centre de référence sur les agents tératogènes (CRAT) (pas disponible au 5 mai 2022)
- IMGT/mAb-DB pour tixagevimab et cilgavimab
- HeTOP[2] pour tixagevimab et cilgavimab
Remarque :
Dernière mise à jour : 6 mai 2022
Relecture par : Pr C. Carnoy