Necitumumab (PORTRAZZA®)
Attention :
L'autorisation de mise sur le marché du médicament a été retirée le 18 février 2021 à demande du titulaire de l'autorisation de mise sur le marché
Structure : IgG1, humain
Code ATC : L01
Nomenclature Ge : IgG1κ G1e6
Cible: human epidermal growth factor receptor 1 (EGFR)
Mode d'administration : IV
Date de la première AMM : EMA 2016 / FDA 2015
Laboratoires : Eli Lilly Nederland B.V.
Indications : en association à une chimiothérapie par gemcitabine et cisplatine, dans le traitement des patients adultes atteints d'un cancer bronchique non à petites cellules (CBNPC) de type épidermoïde localement avancé ou métastatique, exprimant le récepteur du facteur de croissance épidermique (EGFR), qui n'ont pas reçu de chimiothérapie antérieure pour cette pathologie
Prix indicatif : XXX
Usage : xxx
Posologies :
xxx
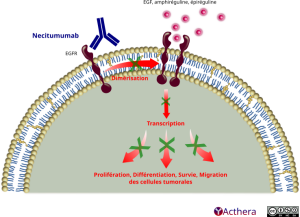
Mécanisme d'action :
La fixation du necitumumab aux EGFR entraîne le blocage de la phosphorylation des récepteurs induite par le ligand et de la signalisation en aval. Des études in vitro ont également démontré que le necitumumab inhibe la prolifération des cellules tumorales dépendantes de l'EGFR.
Effets indésirables les plus fréquents:
Contre-indications :
Principales références :
- Lien vers Human medicine European public assessment report (EPAR)