Avelumab (BAVENCIO®)
Autre nom : MSB0010718C
Structure : AcM humain, IgG1
Code ATC : L01FF04
Nomenclature Ge : IgG1λ G1e0
Cible: PD-L1
Mode de production : Produit dans des cellules ovariennes de hamster chinois par la technique de l’ADN recombinant.
Forme galénique : Solution à diluer pour perfusion 20 mg/mL
Mode d'administration : IV
Conservation : D'un point de vue microbiologique, après ouverture, le médicament doit être dilué et perfusé immédiatement. Après préparation de la solution pour perfusion : la stabilité chimique et physique de la solution diluée a été démontrée
- 96h dans du NaCl 0,9% entre 2 et 8°C.
- 72h dans du NaCl 0,9% à t° ambiante
- 24h dans du NaCl 0,45% entre 2 et 8°C ou à t° ambiante.
Date de la première AMM : FDA Mars 2017 - EMA Septembre 2017
Laboratoires : Merck Serono Europe Limited
Indications :
- Carcinome à cellules de Merkel (CCM) : En monothérapie pour le traitement de patients atteints de carcinome à cellules de Merkel (CCM) métastatique de l'adulte.
- Carcinome urothélial (CU) : En monothérapie pour le traitement d’entretien de première ligne des patients adultes atteints de carcinome urothélial (CU) à un stade localement avancé ou métastatique, dont la maladie n’a pas progressé après la chimiothérapie à base de sel de platine.
- Carcinomes à cellules rénales : En association avec l'axitinib dans le traitement de première ligne des patients adultes atteints de carcinome à cellules rénales (CCR) à un stade avancé.
Prix indicatif : 651,340 euros le flacon de 10 mL
Usage : Médicament réservé à l'usage hospitalier. Prescription réservée aux spécialistes en oncologie et aux médecins compétents en cancérologie. Médicament nécessitant une surveillance particulière pendant le traitement.
Posologies : La dose recommandée de Bavencio est de 800 mg à administrer pendant 60 minutes toutes les 2 semaines.
Mécanisme d'action :
Avelumab se lie au PD-L1 et bloque l'interaction entre le PD-L1 et ses récepteurs, PD-1 (protéine de mort programmée 1) et B7.1. Cela conduit à la suppression des effets inhibiteurs du PD-L1 sur les lymphocytes T CD8+ cytotoxiques, rétablissant ainsi les réponses anti-tumorales des lymphocytes T. Il a également été montré qu'avelumab induisait une lyse directe des cellules tumorales par les cellules Natural Killer (NK) via la cytotoxicité à médiation cellulaire dépendante des anticorps (ADCC).
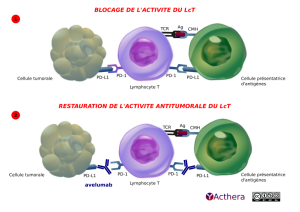
L'image est divisée en deux parties. La première situation est sans l’intervention d’avelumab, la seconde avec.
Première situation "BLOCAGE DE L'ACTIVITÉ DU LcT", montre une cellule tumorale, à gauche, un lymphocyte T, au centre, et une cellule présentatrice d'antigènes, à droite.
Les protéines PD-L1 présentes sur la cellule tumorale, à gauche, et la cellule présentatrice d'antigènes, à droite, interagissent avec les récepteurs PD-1 présents de chaque coté du lymphocyte T, au centre. Cela entraîne un blocage de l'activité du lymphocyte T. Le TCR présent sur le Lymphocyte T est mis en relation avec le CMH par l’A g (antigène).
Deuxième situation "RESTAURATION DE L'ACTIVITÉ ANTITUMORALE DU LcT", montre un schéma similaire, mais avec l’intervention de l'avelumab (A c M humain I g G 1). Il se lie à PD-L1 de la cellule tumorale et de la cellule présentatrice d’antigènes, empêchant ainsi l’interaction avec PD-1 sur le lymphocyte T et restaurant ainsi l'activité antitumorale du lymphocyte T.
Effets indésirables les plus fréquents : fatigue (32,4 %), des nausées (25,1 %), des diarrhées (18,9 %), une diminution de l'appétit (18,4 %), une constipation (18,4 %), des réactions liées à la perfusion (17,1 %), une perte de poids (16,6 %) et des vomissements (16,2 %)
Contre indications : Hypersensibilité à la substance
Principales références :
Liens :
- Avis de la HAS sur Bavencio
- Lien vers Human medicine European public assessment report (EPAR)
- FDA
- Base de données publique des médicaments
- ANSM
- Meddispar - pas de données au 13 mars 2023
- CRAT -pas de données au 13 mars 2023
- Vidal
- IMGT/DB
- HeTop
Remarque :
Dernière mise à jour : Mars 2023
Par : Mathilde GLAZIOU