Evolocumab (REPATHA®)
Structure : AcM humain, IgG2
Code ATC : C10AX13
Nomenclature Ge : IgG2λ G2e0
Cible: proprotein convertase subtilisin kexin type 9 (PCSK9)
Mode de production : produit dans des cellules d'ovaires d'hamsters chinois (CHO) par la technique de l'ADN recombinant
Forme galénique : Solution pour injection
- Seringues pré-remplies de 140 mg
- Stylos pré-remplis de 140 mg
- Cartouches de 420 mg (minidoseur automatique) permettant une injection en 9 minutes.
Mode d'administration : SC
Conservation : Au réfrigérateur entre 2 et 8 °C. Une fois sorti du réfrigérateur, Repatha peut être conservé à température ambiante (jusqu'à 25 °C) dans son emballage d'origine et doit être utilisé dans un délai d'un mois.
Date de la première AMM : EMA juillet 2015 / FDA Août 2015
Laboratoire : AMGEN
Indications :
- Hypercholestérolémie et dyslipidémie mixte chez l'adulte
Repatha est indiqué chez les adultes atteints d'hypercholestérolémie primaire (familiale hétérozygote et non familiale) ou de dyslipidémie mixte, et chez les patients pédiatriques âgés de 10 ans et plus atteints d'hypercholestérolémie familiale hétérozygote ou non familiale.
d'une hypercholestérolémie familiale hétérozygote, en complément d'un régime alimentaire
- En association avec une statine ou avec d'autres thérapies hypolipémiantes chez les patients qui ne peuvent pas
d'atteindre les objectifs de LDL-C avec la dose maximale tolérée d'une statine
- Seul ou en association avec d'autres thérapies hypolipémiantes chez les patients qui ne tolèrent pas les statines,
ou pour lesquels une statine est contre-indiquée.
- Hypercholestérolémie familiale homozygote
Repatha est indiqué chez les adultes et les enfants âgés de 10 ans et plus atteints d'hypercholestérolémie familiale homozygote en association avec d'autres traitements hypolipidémiants.
- Maladie cardiovasculaire athéroscléreuse établie
Repatha est indiqué chez les adultes atteints d'une maladie cardiovasculaire athéroscléreuse établie (infarctus du myocarde, accident vasculaire cérébral ou maladie artérielle périphérique) afin de réduire le risque cardiovasculaire en abaissant le taux de LDL-C en complément de la correction d'autres facteurs de risque :
- en association avec la dose maximale tolérée d'une statine, avec ou sans autres thérapies hypolipémiantes ou, en association avec la dose maximale tolérée d'une statine.
- seul ou en association avec d'autres thérapies hypolipémiantes chez les patients qui ne tolèrent pas les statines, ou pour lesquels une statine est contre-indiquée.
Prix indicatif 2024: 216.1 euros pour 1 stylo prérempli à 140 mg / ml (220,05 euros en 2020).
Usage : Prescription initiale annuelle réservée aux spécialistes en cardiologie, en endocrinologie, diabète et maladies métaboliques ou en médecine interne, médecine vasculaire ou neurologie. Renouvellement non restreint. Disponible en ville.
Posologies :
- Hypercholestérolémie primaire et dyslipidémie : 140 mg / 2 semaines ou 420 mg / mois ou 420 mg/2 semaines selon la situation clinique.
- Hypercholestérolémie familiale homozygote chez l'adulte et l'adolescent à partir de 12 ans : Dose initiale recommandée = 420 mg / mois. Après 12 semaines de traitement, en l'absence de réponse cliniquement significative, la fréquence d'administration peut être portée à 420 mg / 2 semaines.
Mécanisme d'action :
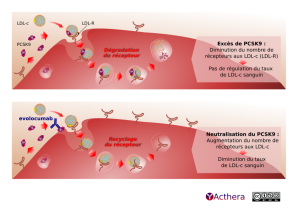
PCSK9 se lie aux récepteurs au LDL-C présents à la surface des hépatocytes et favorise leur dégradation dans le foie. Les récepteurs au LDL-C captent les LDL-C circulants. Par conséquent, la diminution du nombre des récepteurs au LDL-C par PCSK9 entraîne une augmentation du LDL-C dans le sang. En empêchant PCSK9 de se lier aux récepteurs au LDL-C, l'alirocumab augmente le nombre de récepteurs disponibles pour capter le LDL-C circulant et permet donc de diminuer le taux de LDL-C dans le sang.
Effets indésirables les plus fréquents : rhinopharyngite, infection des voies respiratoires supérieures, dorsalgies, arthralgies, grippe, nausées, réaction au point d'injection (érythème, douleur, ecchymose)
Contre-indications : Hypersensibilité à l'un des excipients (Proline, Acide acétique glacial, Polysorbate 80, Hydroxyde de sodium)
Utilisation chez la femme enceinte : Repatha ne doit pas être utilisé pendant la grossesse, sauf si l'état clinique de la femme nécessite un traitement par evolocumab
Principales références :
- Nasso G, Vignaroli W, Amodeo V, Bartolomucci F, Larosa C, Contegiacomo G, Demola MA, Girasoli C, Valenzano A, Fiore F, Bonifazi R, Triggiani V, Vitobello V, Errico G, Lamanna A, Hila D, Loizzo T, Franchino R, Sechi S, Valenti G, Diaferia G, Brigiani MS, Arima S, Angelelli M, Curcio A, Greco F, Greco E, Speziale G, Santarpino G. Evolocumab Treatment in Dyslipidemic Patients Undergoing Coronary Artery Bypass Grafting: One-Year Safety and Efficacy Results. J Clin Med. 2024 May 19;13(10):2987. doi: 10.3390/jcm13102987. PMID: 38792527; PMCID: PMC11121999.
- Pasta A, Cremonini AL, Pisciotta L, Buscaglia A, Porto I, Barra F, Ferrero S, Brunelli C, Rosa GM. PCSK9 inhibitors for treating hypercholesterolemia. Expert Opin Pharmacother. 2020 Feb;21(3):353-363. doi: 10.1080/14656566.2019.1702970. Epub 2020 Jan 1. PMID: 31893957.
- Roth EM, Davidson MH. PCSK9 Inhibitors: Mechanism of Action, Efficacy, and Safety. Rev Cardiovasc Med. 2018;19(S1):S31-S46. doi: 10.3909/ricm19S1S0002. PMID: 30207556.
- Kasichayanula S, Grover A, Emery MG, Gibbs MA, Somaratne R, Wasserman SM, Gibbs JP. Clinical Pharmacokinetics and Pharmacodynamics of Evolocumab, a PCSK9 Inhibitor. Clin Pharmacokinet. 2018 Jul;57(7):769-779. doi: 10.1007/s40262-017-0620-7. PMID: 29353350; PMCID: PMC5999140.
- Sabatine MS, Giugliano RP, Wiviott SD, Raal FJ, Blom DJ, Robinson J, Ballantyne CM, Somaratne R, Legg J, Wasserman SM, Scott R, Koren MJ, Stein EA; Open-Label Study of Long-Term Evaluation against LDL Cholesterol (OSLER) Investigators. Efficacy and safety of evolocumab in reducing lipids and cardiovascular events. N Engl J Med. 2015 Apr 16;372(16):1500-9. doi: 10.1056/NEJMoa1500858. Epub 2015 Mar 15. PMID: 25773607.
- Markham A. Evolocumab: First Global Approval. Drugs. 2015 Sep;75(13):1567-73. doi: 10.1007/s40265-015-0460-4. PMID: 26323342.
- Blom DJ, Hala T, Bolognese M, Lillestol MJ, Toth PD, Burgess L, Ceska R, Roth E, Koren MJ, Ballantyne CM, Monsalvo ML, Tsirtsonis K, Kim JB, Scott R, Wasserman SM, Stein EA; DESCARTES Investigators. A 52-week placebo-controlled trial of evolocumab in hyperlipidemia. N Engl J Med. 2014 May 8;370(19):1809-19. doi: 10.1056/NEJMoa1316222. Epub 2014 Mar 29. PMID: 24678979.
Liens :
- Lien vers Human medicine European public assessment report (EPAR)
- Fiche AMGEN destinée aux patients
- Avis de la HAS sur Repatha
- FDA
- Bases de données des médicaments
- Vidal
- CRAT : pas de données au 06/06/2
- IMGT/DB
- HeToP
Note :
mise à jour des références par Pr C. Carnoy le 6/06/24
mise à jour 05/23 par Mathilde GLAZIOU