Vilobelimab (GOHIBIC®)
Structure : AcM chimérique de type IgG4.
Code ATC : L04AJ10
Nomenclature Ge : xxx
Cible: C5a
Mode de production : produit dans des cellules d’ovaire de hamster chinois (CHO) par la technologie de l’ADN recombinant
Forme galénique : Chaque flacon contient 200 mg de vilobélimab dans 20 ml. Après dilution, chaque ml de solution contient 3,2 mg de vilobélimab
Mode d'administration : IV
Date de la première AMM : FDA XXX / EMA janvier 2025
Laboratoire : InflaRx GmbH
Indications :Traitement du syndrome de détresse respiratoire aiguë (SDRA) induit par le SARS-CoV-2 chez les adultes qui reçoivent des corticostéroïdes systémiques dans le cadre de la prise en charge standard et qui reçoivent une ventilation mécanique invasive [avec ou sans oxygénation par membrane extracorporelle (ECMO)]
Prix indicatif (année) : XXX
Posologies :
La dose recommandée est de 800 mg administrés par perfusion intraveineuse après dilution, pour un maximum de 6 (six) doses sur la période de traitement. La première perfusion doit être administrée dans les 48 heures suivant le début de la ventilation mécanique (jour 1 du traitement); les perfusions suivantes sont administrées aux jours 2, 4, 8, 15 et 22 du traitement, aussi longtemps que le patient est hospitalisé, même s’il est libéré de l’unité de soins intensifs.
Mécanisme d'action :
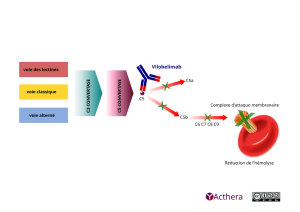
Le vilobelimab se lie à un composant soluble du complément humain appelée C5a, ce qui bloque son action. En général, les taux initiaux de C5a sont élevés chez ces patients par rapport aux valeurs moyennes observées chez des individus en bonne santé et le traitement par le vilobélimab a réduit les taux initiaux moyens de C5a
Visuel du mécanisme d'action de l'anticorps monoclonal chimérique Vilobelimab.
Effets indésirables les plus fréquents : Infections telles que la pneumonie, infection à l’herpès, aspergillose bronchopulmonaire et septicémie (se référer au RCP pour avoir la liste complète des effets indésirables).
Contre-indications : Hypersensibilité à la substance active ou à l’un des excipients.
Principales références :
- Nadig N, Bhimraj A, Cawcutt K, Chiotos K, Dzierba AL, Kim AY, Martin GS, Pearson JC, Shumaker AH, Baden LR, Bedimo R, Cheng VC, Chew KW, Daar ES, Glidden DV, Hardy EJ, Johnson S, Li JZ, MacBrayne C, Nakamura MM, Riley L, Shafer RW, Shoham S, Tebas P, Tien PC, Loveless J, Falck-Ytter Y, Morgan RL, Gandhi RT. 2025 Clinical Practice Guideline Update by the Infectious Diseases Society of America on the Treatment and Management of COVID-19: Vilobelimab. Clin Infect Dis. 2025 May 22:ciaf235. doi: 10.1093/cid/ciaf235. Epub ahead of print. PMID: 40402009.
- Vlaar APJ, Witzenrath M, van Paassen P, Heunks LMA, Mourvillier B, de Bruin S, Lim EHT, Brouwer MC, Tuinman PR, Saraiva JFK, Marx G, Lobo SM, Boldo R, Simon-Campos JA, Cornet AD, Grebenyuk A, Engelbrecht JM, Mukansi M, Jorens PG, Zerbib R, Rückinger S, Pilz K, Guo R, van de Beek D, Riedemann NC; PANAMO study group. Anti-C5a antibody (vilobelimab) therapy for critically ill, invasively mechanically ventilated patients with COVID-19 (PANAMO): a multicentre, double-blind, randomised, placebo-controlled, phase 3 trial. Lancet Respir Med. 2022 Dec;10(12):1137-1146. doi: 10.1016/S2213-2600(22)00297-1. Epub 2022 Sep 7. PMID: 36087611; PMCID: PMC9451499.
- van Amstel RBE, Slim MA, Lim EHT, Rückinger S, Seymour CW, Burnett BP, Bos LDJ, van Vught LA, Riedemann NC, van de Beek D, Vlaar APJ; PANAMO Study Group. Heterogeneity of treatment effect of vilobelimab in COVID-19: a secondary analysis of a randomised controlled trial. Crit Care. 2024 Jun 28;28(1):210. doi: 10.1186/s13054-024-05004-z. PMID: 38943192; PMCID: PMC11214248.
- Vlaar APJ, Lim EHT, de Bruin S, Rückinger S, Pilz K, Brouwer MC, Guo RF, Heunks LMA, Busch MH, van Paassen P, Riedemann NC, van de Beek D. The anti-C5a antibody vilobelimab efficiently inhibits C5a in patients with severe COVID-19. Clin Transl Sci. 2022 Apr;15(4):854-858. doi: 10.1111/cts.13213. Epub 2022 Jan 14. PMID: 35029045; PMCID: PMC9010279.
Liens :
- Human medicine European public assessment report (EPAR)
- HAS (pas de données au 23/06/2025)
- Base de données publique des médicaments (pas de données au 23/06/2025)
- ANSM (pas de données au 23/06/2025)
- Meddispar (pas de données au 23/06/2025
- Vidal (pas de données au 23/06/2025)
- Centre de référence sur les agents tératogènes (CRAT) (pas de données au 23/06/2025)
Note :
Création de la fiche : Lorie Nguyen
Dernière mise à jour : 23 juin 2025
Relecture par : Pr C. Carnoy