Relatlimab - nivolumab (OPDUALAG®)
Autres noms : relatlimab-rmbw ;
Structure : IgG4 kappa pour relatlimab et nivolumab
Code ATC : L01XY03
Nomenclature Ge : xxx
Cible: LAG3 (lymphocyte-activation gene-3) pour relatlimab et PD1 (programmed death-1) pour nivolumab
Mode de production : Produits sur des cellules ovariennes de hamster chinois, par la technologie de l’ADN recombinant
Forme galénique : Flacon de 20 mL contenant 240 mg de nivolumab et 80 mg de relatlimab. Solution à diluer pour perfusion.
Mode d'administration : IV
Date de la première AMM : EMA septembre 2022 / FDA mars 2022
Laboratoires : Bristol-Myers Squibb
Indications : Première ligne de traitement du mélanome avancé (non résécable ou métastatique) chez les adultes et les adolescents âgés de 12 ans et plus avec une expression de PD-L1 au niveau des cellules tumorales inférieure à 1 %
Prix indicatif (année) : XXX
Posologies : La dose recommandée pour les adultes et les adolescents âgés de 12 ans et plus est de 480 mg de nivolumab et 160 mg de relatlimab toutes les 4 semaines, administré en perfusion intraveineuse pendant 30 minutes. Cette dose est établie pour les patients adolescents pesant au moins 30 kg
Mécanisme d'action :
Opdualag est une association à dose fixe de nivolumab, un anti-PD-1 , et de relatlimab, un anti-LAG-3. La liaison des ligands PD-1, PD-L1 et PD-L2 au récepteur PD-1 situé sur les lymphocytes T inhibe la prolifération des lymphocytes T et la production de cytokines. La régulation à la hausse des ligands PD-1 survient dans certaines tumeurs et la transmission du signal par cette voie peut contribuer à l’inhibition de la surveillance immunitaire des lymphocytes T actifs des tumeurs. Le nivolumab se lie au récepteur PD-1, bloque son interaction avec ses ligands PD-L1 et PD-L2, et limite l’inhibition médiée par la voie PD-1 de la réponse immunitaire, y compris de la réponse immunitaire anti-tumorale.
Le relatlimab se lie au récepteur LAG-3, bloque son interaction avec ses ligands, y compris avec le MHC II, et limite l’inhibition médiée par la voie LAG-3 de la réponse immunitaire. L’antagonisme de cette voie favorise la prolifération des lymphocytes T et la libération de cytokines. L’association du nivolumab (anti-PD-1) et du relatlimab (anti-LAG-3) entraîne une activation accrue des lymphocytes T par rapport à l’activité des deux anticorps seuls. Dans des modèles de tumeurs murines syngéniques, le blocage de LAG-3 potentialise l’activité anti-tumorale du blocage de PD-1, inhibant ainsi la croissance de la tumeur et favorisant sa régression.
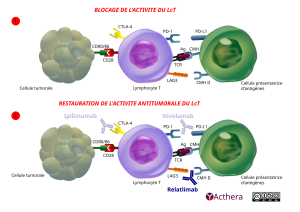
Illustration de l’action de blocage par le relatlimab de la liaison de PD-1 aux ligands PD-L1 et PD-L2 qui permet la réactivation de la réponse antitumorale du LcT.
L'image est divisée en deux parties.
1. La première supérieure, intitulée "BLOCAGE DE L'ACTIVITÉ DU LcT", montre une cellule tumorale à gauche, un lymphocyte T au centre, et une cellule présentatrice d'antigènes à droite.
Les protéines PD-L2 et PD-L1 présentes sur la cellule tumorale, à gauche, et PD-L1 sur la cellule présentatrice d'antigènes, à droite, interagissent avec les trois récepteur PD-1 du lymphocyte T situé au centre de l’illustration. Deux récepteurs PD-1 sont sur le côté gauche, le troisième à droite. Cela entraîne un blocage de l'activité du lymphocyte T. Le TCR présent sur le Lymphocyte T est mis en relation avec le CMH par l’A g (antigène)
2. La deuxième partie, intitulée "RESTAURATION DE L'ACTIVITÉ ANTITUMORALE DU LcT", montre un schéma similaire, mais avec l’intervention de relatlimab (A c M humain I g G 1). Ce dernier se lie à PD-L2 et PD-L1 de la cellule tumorale et au PD-L1 de la cellule présentatrice d’antigènes et empêche ainsi l’interaction avec PD-1 sur le lymphocyte T, permettant de restaurer l'activité antitumorale du lymphocyte T.
Effets indésirables les plus fréquents : Les effets indésirables les plus fréquents sont les suivants : fatigue (41 %), douleurs musculo-squelettiques (32 %), éruption cutanée (29 %), arthralgie (26 %), diarrhée (26 %), prurit (26 %), céphalées (20 %), nausées (19 %), toux (16 %), appétit diminué (16 %), hypothyroïdie (16 %), douleurs abdominales (14 %), vitiligo (13 %), fièvre (12 %), constipation (11 %), infection des voies urinaires (11 %), dyspnée (10 %) et vomissements (10 %).
Les effets indésirables graves les plus fréquents sont les suivants : insuffisance surrénalienne (1,4 %), anémie (1,4 %), dorsalgie (1,1 %), colite (1,1 %), diarrhée (1,1 %), myocardite (1,1 %), pneumonie (1,1 %) et infection des voies urinaires (1,1 %). L’incidence des effets indésirables de grade 3 à 5 chez les patients atteints d’un mélanome avancé (non résécable ou métastatique) était de 43 % pour le nivolumab en association avec le relatlimab et de 35 % chez les patients traités par nivolumab seul.
(se référer au RCP pour avoir la liste complète des effets indésirables)
Contre-indications : Hypersensibilité aux substances actives ou à l’un des excipients
Principales références :
- Paik J. Nivolumab Plus Relatlimab: First Approval. Drugs. 2022 Jun;82(8):925-931. doi: 10.1007/s40265-022-01723-1. PMID: 35543970.
- Amaria RN, Postow M, Burton EM, Tezlaff MT, Ross MI, Torres-Cabala C, Glitza IC, Duan F, Milton DR, Busam K, Simpson L, McQuade JL, Wong MK, Gershenwald JE, Lee JE, Goepfert RP, Keung EZ, Fisher SB, Betof-Warner A, Shoushtari AN, Callahan M, Coit D, Bartlett EK, Bello D, Momtaz P, Nicholas C, Gu A, Zhang X, Korivi BR, Patnana M, Patel SP, Diab A, Lucci A, Prieto VG, Davies MA, Allison JP, Sharma P, Wargo JA, Ariyan C, Tawbi HA. Neoadjuvant relatlimab and nivolumab in resectable melanoma. Nature. 2022 Nov;611(7934):155-160. doi: 10.1038/s41586-022-05368-8. Epub 2022 Oct 26. PMID: 36289334; PMCID: PMC9607737.
- Tawbi HA, Schadendorf D, Lipson EJ, Ascierto PA, Matamala L, Castillo Gutiérrez E, Rutkowski P, Gogas HJ, Lao CD, De Menezes JJ, Dalle S, Arance A, Grob JJ, Srivastava S, Abaskharoun M, Hamilton M, Keidel S, Simonsen KL, Sobiesk AM, Li B, Hodi FS, Long GV; RELATIVITY-047 Investigators. Relatlimab and Nivolumab versus Nivolumab in Untreated Advanced Melanoma. N Engl J Med. 2022 Jan 6;386(1):24-34. doi: 10.1056/NEJMoa2109970. PMID: 34986285; PMCID: PMC9844513.
- Raschi E, Comito F, Massari F, Gelsomino F. Relatlimab and nivolumab in untreated advanced melanoma: insight into RELATIVITY. Immunotherapy. 2023 Feb;15(2):85-91. doi: 10.2217/imt-2022-0172. Epub 2023 Jan 11. PMID: 36628573.
- Li Y, Liang X, Li H, Chen X. Comparative efficacy and safety of immune checkpoint inhibitors for unresectable advanced melanoma: A systematic review and network meta-analysis. Int Immunopharmacol. 2023 Feb;115:109657. doi: 10.1016/j.intimp.2022.109657. Epub 2023 Jan 4. PMID: 36608446.
Liens :
- Human medicine European public assessment report (EPAR)
- Food and drug administration
- HAS : OPDIVO (nivolumab) Pas de données pour relatlimab au 7 février 2023
- Base de données publique des médicaments (pas de données au 7 février 2023)
- ANSM (pas de données au 7 février 2023)
- Meddispar (pas de données au 7 février 2023)
- Centre de référence sur les agents tératogènes (CRAT) (pas de données au 7 février 2023)
- IMGT/mAb-DB : relatlimab - nivolumab
Remarque :
Création de la fiche : Pr C. Carnoy
Dernière mise à jour : 7/02/ 2023
Relecture par : Pr C. Carnoy