Mirikizumab (OMVOH®)
Autres noms : mirikizumab-mrkz
Structure : AcM humanisé de type IgG4 kappa
Code ATC : L04AC24
Nomenclature Ge : xxx
Cible: IL-23p19
Mode de production : Produit dans des cellules ovariennes de hamster chinois (CHO) par la technologie de l'ADN recombinante.
Forme galénique :
- Solution à diluer pour perfusion (300 mg)
- Solution injectable en stylo ou seringue pré-remplie (100 mg)
Mode d'administration : IV/SC
Date de la première AMM : FDA avril 2023 / EMA mai 2023
Laboratoire : Eli Lilly
Indications :
Ce biomédicament est indiqué pour le traitement des patients adultes atteints de rectocolite hémorragique modérément à sévèrement active qui ont eu une réponse inadéquate, une perte de réponse ou une intolérance à un traitement conventionnel ou à un traitement biologique.
Prix indicatif (année) : xxx
Usage : Depuis avril 2024, fait partie des biothérapies pouvant être initiée par un spécialiste en ville (pour l'injection SC)
Posologies :
La dose d’induction est de 300 mg en perfusion IV pendant au moins 30 minutes aux semaines 0, 4 et 8. La dose d'entretien est de 200 mg (c'est-à-dire deux seringues préremplies ou deux stylos préremplis) par injection SC toutes les 4 semaines après la fin du traitement d'induction.
Mécanisme d'action :
Mirikizumab est un anticorps monoclonal humanisé IgG4 anti-interleukine-23 (anti-IL-23) qui se lie sélectivement à la sous-unité p19 de la cytokine humaine IL-23 et inhibe son interaction avec le récepteur de l'IL-23.
L'IL-23, une cytokine régulatrice, affecte la différenciation, l'expansion et la survie des sous-ensembles de cellules T.
Chez l'homme, il a été démontré que le blocage sélectif de l'IL-23 permettait de normaliser la production de ces cytokines.
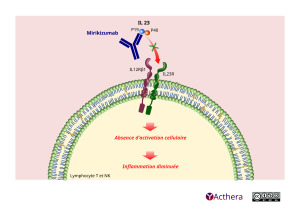
Au centre de l’illustration, une cellule NK ou Lymphocyte T. Au sommet de sa membrane deux récepteurs se font face : à gauche un « IL 12R bêta1 » et un « IL 23R ».
Au dessus de la cellule se trouve l’IL 23. Il se compose de deux sous-unités – deux sphères qui se touchent. À gauche P19 à droite P40.
L’anticorps monoclonal mirikizumab se lie à la sous-unité P19 de l’interleukine 23 (IL 23). L’IL 23 régule, la différentiation, l’expansion et la survie de certaines catégories de cellules dont le lymphocyte-T et certaines sous-populations de cellules de l’immunité innée : IL 17A, IL 17F et IL 22 impliquées dans l’inflammation. Une flèche rouge barrée pointe depuis les sous-unités d’IL 23 sur le récepteur IL 23R, signale que mirikizumab empêche l’IL 23 de se lier à l’IL 23 R.
Dans la cellule sous les récepteurs I-L 12R bêta1 et I-L 23R une flèche pointe en bas sur le texte « Absence d’activation cellulaire ». Sous ce texte une autre flèche désigne plus bas le texte « Inflammation diminuée ». L’action de mirikizumab perturbe le signal et provoque ainsi la baisse de l’inflammation. Le mirikizumab permet une régulation de la production des cytokines IL 23.
Le mirikizumab exerce ses effets cliniques sur le psoriasis en plaques et sur le rhumatisme psoriasique par le blocage de la voie cytokinique de l'IL 23.
Effets indésirables les plus fréquents : infections des voies respiratoires supérieures (7,9 %, le plus
fréquemment des rhinopharyngites), céphalées (3,3 %), éruptions cutanées (1,1 %) et réactions au site d'injection (8,7 %)
(se référer au RCP pour avoir la liste complète des effets indésirables)
Contre-indications : Hypersensibilité à la substance active ou à l'un des excipients, infection active (tuberculose active)
Principales références :
-
-
-
Liens :
- Human medicine European public assessment report (EPAR)
- HAS
- Base de données publique des médicaments - pas de donnée au 12/07/24
- ANSM - pas de donnée au 12/07/24
- Meddispar - pas de donnée au 12/07/24
- Vidal - pas de donnée au 12/07/24
- Centre de référence sur les agents tératogènes (CRAT) - pas de donnée au 12/07/24
Remarque :
Création de la fiche : Pr C. Carnoy
Dernière mise à jour : Juillet 2024
Relecture par : Mathilde Glaziou