Bevacizumab (LYTENAVA®)
Warning :
Fiche en cours de rédaction
Autre nom : bevacizumab-vikg
Structure : AcM humanisé, IgG1k
Code ATC : S01LA08
Nomenclature Ge : IgG1κ G1e0
Cible: VEGF (vascular endothelial growth factor)
Mode de production : produit par la technologie de l'ADN recombinant dans des cellules d'ovaire de Hamster Chinois
Forme galénique : Flacons de 0,3 ml contenant 25mg de bevacizumab.
Mode d'administration : Injection intravitréenne (IVT)
Date de la première AMM : FDA XXX / EMA mai 2024
Laboratoire : Outlook Therapeutics Limited
Indications : Dégénérescence maculaire liée à l'âge (DMLA)
Prix indicatif (année) : XXX
Usage : xxx
Posologies : La dose recommandée est de 1,25 mg administrée par injection intravitréenne toutes les quatre semaines (une fois par mois). Cela correspond à un volume d’injection de 0,05 ml.
Mécanisme d'action :
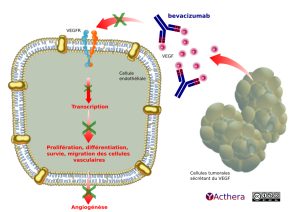
Le bevacizumab se lie sélectivement au VEGF humain et neutralise l'activité biologique par inhibition de la liaison du VEGF à ses récepteurs Flt-1 (VEGFR-1) et KDR (VEGFR-2), situé à la surface des cellules endothéliales. Cette neutralisation permet de réduire la vascularisation des tumeurs et de diminuer l'angiogenèse tumorale, inhibant ainsi la croissance tumorale.
A gauche une cellule endothéliale presque carrée, aux angles arrondis, occupe la moitié de l’illustration. Sur le côté supérieur de sa membrane deux récepteurs V EG F, notés V E G F R. Ils traversent la membrane et se croisent à leur base, dans le cytoplasme.
À la droite de la cellule endothéliale, un groupe de cellules tumorales. Les cellules tumorales sécrètent du V E G F (facteur de croissance vasculaire endothélial). Ce V E G F se dirige sur la cellule endothéliale.
Le bevacizumab (anticorps I g G 1 humanisé) attire les molécules de V E G F produites par les cellules tumorales. Une flèche courbe superposée par une croix pointe depuis le bevacizumab vers le V E G F R de la cellule endothéliale. Elle signale que le contact avec les V E G F R est empêché.
Dans la cellule endothéliale sous le V E G F R « une flèche superposée d’une croix » pointe plus bas sur le mot « Transcription ». Sous « Transcription » une autre « flèche barrée par une croix » pointe sur les termes « Prolifération, différentiation, survie, migration des cellules vasculaires ». De là une nouvelle « flèche surmontée d’une croix » descend sur « Angiogénèse ». L’ensemble des processus est interrompu par l’intervention du bevacizumab sur le V E G F.
Effets indésirables les plus fréquents : Les effets indésirables les plus fréquemment rapportés étaient les suivants: hémorragie conjonctivale (5,0 %), corps flottants vitréens (1,5 %), douleur oculaire (1,2 %) et augmentation de la pression intraoculaire (1,2 %). Les effets indésirables moins fréquemment rapportés, mais plus graves, étaient les suivants: augmentation de la pression intraoculaire (0,6 %), cécité transitoire (0,3 %), endophtalmie (0,3 %), inflammation intraoculaire (0,3 %).
Contre-indications :
-Hypersensibilité à la substance active ou à l’un des excipients
-Patients présentant une infection oculaire ou périoculaire active ou suspectée.
-Patients présentant une inflammation intraoculaire active sévère.
Principales références :
-
-
-
-
Liens :
- Human medicine European public assessment report (EPAR)
- HAS
- Base de données publique des médicaments
- ANSM
- Meddispar
- Vidal
- Centre de référence sur les agents tératogènes (CRAT)
Note :
Création de la fiche : Pr C. Carnoy
Dernière mise à jour :
Relecture par :