Bevasizumab (AVZIVI®) Biosimilaire
Attention :
Fiche en cours de rédaction
Autre nom : bevacizumab-tnjn
Structure : AcM humanisé, IgG1k
Code ATC : L01XC07
Nomenclature Ge : IgG1κ G1e0
Cible: VEGF (vascular endothelial growth factor)
Mode de production : produit par la technologie de l'ADN recombinant dans des cellules d'ovaire de Hamster Chinois
Forme galénique : Flacons de 4 ml ou 16 ml contenant respectivement 100 mg et 400 mg de bevacizumab. Chaque ml de solution à diluer contient 25 mg de bevacizumab.
Mode d'administration : IV perfusion de 90 min, pas en bolus
Date de la première AMM : FDA XXX / EMA Juillet 2024
Laboratoires : FGK Representative Service GmbH
Indications :
- Cancer colorectal métastasique : en association à une chimiothérapie à base de fluoropyrimidine chez les patients adultes (étude AVF2107g).
- Cancer du sein métastasique :
En association au paclitaxel, en première ligne.
En association à la capécitabine, en première ligne.
Non à petites cellules en association à une chimiothérapie à base de sels de platine, dans le traitement de première ligne pour des cancers avancés et non opérables, métastatiques ou en rechute
Non à petites cellules non épidermoïdes, en association à l'erlotinib, en première ligne pour des cancers avancés et non opérables, métastatiques ou en rechutes, et présentant des mutations activatrices de l'EGFR.
- Cancer du rein (avancé et/ou métastatique) : En association à l'interféron alfa-2a, en traitement de première ligne.
- Cancer de l'ovaire avancé, des trompes de Fallope ou péritonéal primitif :
En association au carboplatine et au paclitaxel, en première ligne.
En association au carboplatine et à la gemcitabine en première récidive
En association au paclitaxel, au topotécan ou à la doxorubicine liposomale pégylée en rechute
- Carcinome du col de l'utérus persistant, en rechute ou métastatique :
En association au paclitaxel et au cisplatine
En association au paclitaxel et au topotécan
Prix indicatif (année) : XXX
Usage : réservé à l'usage hospitalier. Prescription réservée aux spécialistes en cancérologie, oncologie médicale.
Posologies :
Cancer colo-rectal : 5 ou 10 mg/kg toutes les 2 semaines ou 7,5 mg/kg ou 15 mg/kg une fois toutes les 3 semaines en IV.
Cancer du sein : 10 mg/kg toutes les 2 semaines ou 15 mg/kg toutes les 3 semaines en IV.
Cancer bronchique : 15 mg/kg toutes les 3 semaines
Cancer du rein : 10 mg/kg toutes les 2 semaines
Cancer de l'ovaire : 10 mg/kg toutes les 2 semaines ou 15 mg/kg toutes les 3 semaines
Cancer du col de l'utérus : 15 mg/kg toutes les 3 semaines
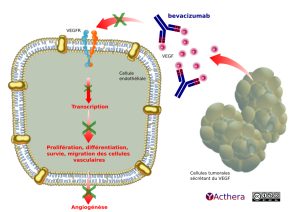
Mécanisme d'action :
Le bevacizumab se lie sélectivement au VEGF humain et neutralise l'activité biologique par inhibition de la liaison du VEGF à ses récepteurs Flt-1 (VEGFR-1) et KDR (VEGFR-2), situé à la surface des cellules endothéliales. Cette neutralisation permet de réduire la vascularisation des tumeurs et de diminuer l'angiogenèse tumorale, inhibant ainsi la croissance tumorale.
Effets indésirables les plus fréquents :
Les effets indésirables les plus graves étaient :
• Des perforations gastro-intestinales.
• Des hémorragies, dont des hémorragies pulmonaires/hémoptysies, plus fréquentes chez les patients atteints d’un cancer bronchique non à petites cellules.
• Des thromboembolies artérielles.
Dans l’ensemble des études cliniques, les effets indésirables les plus fréquemment observés chez les patients recevant du bévacizumab étaient : hypertension artérielle, fatigue ou asthénie, diarrhée et douleur abdominale.
Les analyses des données cliniques de tolérance suggèrent que la survenue d’une hypertension artérielle et d’une protéinurie lors du traitement par bévacizumab sont probablement dose dépendantes.
Contre-indications : hypersensibilité au médicament, grossesse et allaitement.
Principales références :
-
-
-
-
Liens :
- Human medicine European public assessment report (EPAR)
- HAS
- Base de données publique des médicaments
- ANSM
- Meddispar
- Vidal
- Centre de référence sur les agents tératogènes (CRAT)
- IMGT/mAb-DB
- Vidéos d'aide à l'administration du .... en stylo et en seringue (français)
Remarque :
Création de la fiche : Pr C. Carnoy
Dernière mise à jour :
Relecture par :