Ustekinumab (EKSUNBI®) - Biosimilaire
Attention :
Le 19 août 2025, la Commission européenne a retiré l'autorisation de mise sur le marché d'Eksunbi (ustekinumab) dans l'Union européenne (UE). Ce retrait a été effectué à la demande du titulaire de l'autorisation de mise sur le marché, Samsung Bioepis NL B.V., qui a informé la Commission européenne de sa décision de ne pas commercialiser le produit dans l'UE pour des raisons commerciales.
Structure : AcM humain, IgG1k
Code ATC : L04AC05
Nomenclature Ge : xxx
Cible: sous unité p40 de l'IL-12 et de l'IL-23
Mode de production : produit par une lignée de cellules d’ovaires de hamster chinois en utilisant une technique d’ADN recombinant.
Forme galénique :
- flacon contenant 130 mg d'ustekinumab à diluer dans 26 mL (5 mg/mL).
- solution injectable en seringue préremplie à 45 mg et 90 mg d'ustekinumab (disponible en ville)
Mode d'administration : IV
Date de la première AMM : FDA XXX / EMA septembre 2024
Laboratoire : Samsung Bioepis
Indications :
- Psoriasis en plaques : traitement du psoriasis en plaques modéré à sévère chez l'adulte qui n'a pas répondu, ou qui présente une contre-indication, ou qui est intolérant aux autres traitements systémiques dont la ciclosporine, le méthotrexate (MTX) ou la puvathérapie (psoralène et UVA)
- Psoriasis en plaques de la population pédiatrique : traitement du psoriasis en plaques modéré à sévère chez l'enfant et l'adolescent âgé de 6 ans et plus, en cas de réponse insuffisante ou d'intolérance aux autres traitements systémiques ou aux photothérapies (les stylos n'ont pas cette indication).
- Rhumatisme psoriasique : seul ou en association avec le méthotrexate (MTX), est indiqué dans le traitement du rhumatisme psoriasique actif chez l'adulte lorsque la réponse à un précédent traitement de fond antirhumatismal non-biologique (DMARD) a été inadéquate
- Maladie de Crohn : traitement de la maladie de Crohn active modérée à sévère chez les patients adultes présentant une réponse insuffisante, une perte de réponse ou une intolérance à un traitement conventionnel ou par anti-TNFα, ou qui présentent une contre-indication médicale à ces traitements.
- Rectocolite hémorragique : traitement de la rectocolite hémorragique active modérée à sévère chez les patients adultes présentant une réponse insuffisante, une perte de réponse ou une intolérance à un traitement conventionnel ou à un agent biologique, ou qui présentent une contre-indication médicale à ces traitements.
Prix indicatif (année) : XXX
Posologies : La dose initiale d'ustekinumab est de 45 mg suivie d'une dose de 45 mg 4 semaines plus tard, puis une dose de 45 mg toutes les 12 semaines
Mécanisme d'action :
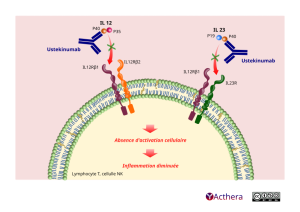
Les épisodes inflammatoires observés dans le psoriasis et les MICI sont en partie liés à un trouble de régulation de l'IL-12 et de l'IL-23, deux cytokines pro-inflammatoires. L'ustékinumab, est dirigé contre la sous unité p40 commune à l'IL-12 et à l'IL-23. L'ustékinumab empêche la fixation de ces interleukines au récepteur IL-12Rβ1 présent à la surface des cellules immunitaires, limitant ainsi l'activation des cellules NK, des LT CD4+.
Au centre de l’illustration, une cellule NK ou Lymphocyte T. Sur sa membrane deux paires de récepteurs, une à gauche composée d’« IL 12R bêta1 » et d’« IL 12R bêta2 » , une à droite composée d’« IL 12R bêta1 » et d’« IL 23R ».
Au dessus de chaque paire de récepteurs se trouve deux interleukines. IL 12 au-dessus d’« IL 12R bêta1 » et d’ « IL 12R bêta2 ». « IL 23 » au dessus d’« IL 12R bêta1 » et d’« IL 23R ».
Chaque Interleukine se compose de deux sous unités – deux sphères qui se touchent – P40 à gauche, P35 à droite font l’IL12. Et P19 à gauche, P40 à droite font l’IL 23.
À gauche ustekinumab (un anticorps humain I-g-G-1) se lie au P40 de l’IL 12 tandis qu’à droite ustekinumab se lie au P40 de l’IL 23.
Sous IL 12 une flèche superposée d’une croix pointe vers IL 12 R béta 1. Sous IL 23 une flèche surmonté d’une croix désigne IL 23 R. Ces flèches signifient que l’intervention d’ustekinumab par l’inhibition des sous unités P40, empêche la fixation des cytokines pro inflammatoires IL 12 et IL 23 aux récepteurs IL 12 R béta 1 et IL 23 R. Ce qui limite l’activation du Lymphocyte (ou de la cellule NK ciblée).
Au centre dans la cellule sous les récepteurs une flèche pointe en bas sur le texte « Absence d’activation cellulaire. Sous ce texte une autre flèche désigne plus bas un le texte « Inflammation diminuée ».
Effets indésirables les plus fréquents : infection dentaire, infection des voies respiratoire
Contre-indications : hypersensibilité au médicament, patient avec infection active
Principales références :
-
-
-
-
Liens :
- Human medicine European public assessment report (EPAR)
- HAS
- Base de données publique des médicaments
- ANSM
- Meddispar
- Vidal
- Centre de référence sur les agents tératogènes (CRAT)
- IMGT/mAb-DB
Remarque :
Création de la fiche : Pr C. Carnoy
Dernière mise à jour : 23 septembre 2025
Relecture par :