Elranatamab (ELREXFIO®)
Autres noms : elranatamab-bcmm
Structure : AcM humanizé bispécifique de type IgG2 kappa
Code ATC : non encore attribué
Nomenclature Ge : xxx
Cible: CD3 epsilon et BCMA
Mode de production : Produit à partir de deux lignées cellulaires recombinantes issues d’ovaires de hamster chinois (CHO)
Forme galénique : Solution injectable (en flacon de 40 mg/mL)
Mode d'administration : SC
Date de la première AMM : EMA décembre 2023 / FDA aout 2023
Laboratoire : Pfizer
Indications :
Myélome multiple : Ce biomédicament est indiqué en monothérapie pour le traitement des patients adultes atteints de myélome multiple en rechute et réfractaire, ayant reçu au moins trois traitements antérieurs, incluant un agent immunomodulateur, un inhibiteur du protéasome et un anticorps anti-CD38, et dont la maladie a progressé pendant le dernier traitement.
Prix indicatif : xxx
Usage :
Médicament soumis à prescription restreinte. Prescription hospitalière réservée aux spécialistes en oncologie ou en hématologie ou aux médecins compétents en cancérologie, en oncologie médicale ou en maladies du sang.
Surveillance particulière pendant le traitement. Médicament réservé à l'usage hospitalier.
Posologies :
Les doses recommandées sont des doses croissantes (phase d’escalade de dose) de 12 mg le jour 1 et de 32 mg le jour 4, suivies de doses complètes de 76 mg une fois par semaine, de la Semaine 2 à la Semaine 24.
Pour les patients ayant reçu au moins 24 semaines de traitement par ELREXFIO et ayant obtenu une réponse, l’intervalle entre les doses doit passer à 2 semaines.
Mécanisme d'action :
L’elranatamab est un anticorps bispécifique engageant les lymphocytes T qui se lie au CD3-epsilon sur les lymphocytes T et à l’antigène de maturation des lymphocytes B (BCMA) exprimé sur les plasmocytes, les plasmablastes et les cellules myélomateuse. La liaison de l’elranatamab au BCMA exprimé sur les cellules tumorales et au CD3 exprimé sur les lymphocytes T est indépendante de la spécificité du récepteur des lymphocytes T (TCR) natif ou de la dépendance aux molécules du complexe majeur d’histocompatibilité (CMH) de classe 1. L’elranatamab a activé les lymphocytes T, entraîné la relargage des cytokines pro-inflammatoires et provoqué la lyse des cellules du myélome multiple.
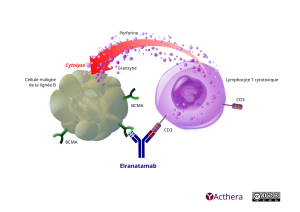
Sur l’illustration la cellule maligne de lignée B exprime à sa surface plusieurs récepteurs BC M A (antigène de maturation des lymphocytes B).
Près d’elle se trouve un « lymphocyte T cytotoxique » et sur sa surface plusieurs CD3 (cluster de différenciation).
Elranatamab (anticorps humanisé I g G 2 kappa) se lie simultanément d’un côté à l’un des CD3 du lymphocyte T, et de l’autre côté à l’un des BC M A présents sur la cellule maligne. Le Lymphocyte activé par elranatamab, génère une réponse cytotoxique. Un flot de granules, composés de « granzyne » et de « perforine » éjecté depuis l’intérieur du lymphocyte T, se dirige sur la cellule maligne. Cette action est la « Cytolyse ». Elle provoque la destruction de la cellule maligne.
Effets indésirables les plus fréquents : Les effets indésirables les plus fréquents sont le syndrome de relargage cytokinique (57,9 %), l’anémie (54,1 %), la neutropénie (44,8 %), la fatigue (44,3 %), l’infection des voies aériennes supérieures (38,8 %), la réaction au site d’injection (38,3 %), la diarrhée (37,7 %), la pneumonie (37,2 %), la thrombopénie (36,1 %), la lymphopénie (30,1 %), la diminution de l’appétit (26,8 %), la fièvre (27,3 %), le rash (26,2 %), l’arthralgie (25,1 %), l’hypokaliémie (23,0 %), les nausées (21,3 %) et la sécheresse cutanée (21,3 %) (se référer au RCP pour avoir la liste complète des effets indésirables).
Contre-indications : Hypersensibilité à la substance active ou à l’un des excipients
Principales références :
-
-
-
-
Liens :
- Human medicine European public assessment report (EPAR)
- HAS
- Base de données publique des médicaments
- ANSM
- Meddispar - pas de donnée au 11/07/24
- Vidal
- Centre de référence sur les agents tératogènes (CRAT) - pas de donnée au 11/07/24
Remarque :
Création de la fiche : Pr C. Carnoy
Dernière mise à jour : Juillet 2024
Relecture par : Mathilde Glaziou