Belantamab mafodotin (BLENREP®)
Attention :
Le comité des médicaments à usage humain (CHMP) de l'EMA a confirmé sa recommandation initiale de ne pas renouveler l'autorisation conditionnelle de mise sur le marché de belantamab mafodotin (BLENREP®), car les données récentes ne confirment pas son efficacité ; les bénéfices de BLENREP® sont donc considérés comme ne l'emportant plus sur les risques.
Structure : AcM humanisé afucosylé de type IgG1κ conjugué au monométhyl auristatine F via un linker (maléimidocaproyl) sur une moyenne de 4 cystéines
Code ATC : L01XC39
Nomenclature Ge : IgG1κ G1e0 conjuguée
Cible: BCMA (B-cell maturation antigen)
Mode de production : Le belantamab est produit par la technique de l’ADN recombinant dans une lignée cellulaire de mammifère (ovaire de hamster chinois)
Forme galénique : Poudre pour solution à diluer pour perfusion (100 mg)
Mode d'administration : IV
Date de la première AMM : FDA Aout 2020 / EMA Aout 2020
Laboratoires et lien vers xxx: GlaxoSmithKline
Indications :
Ce traitement est indiqué en monothérapie pour le traitement des patients adultes atteints de myélome multiple, ayant reçu au moins 4 traitements antérieurs et dont la maladie est réfractaire à au moins un inhibiteur du protéasome, un agent immunomodulateur et un anticorps monoclonal anti-CD38, et dont la maladie a progressé lors du dernier traitement
Prix indicatif (année) : XXX
Usage : Médicament réservé à l’usage hospitalier. Prescription réservée aux spécialistes en oncologie, hématologie, ou aux médecins compétents en cancérologie ou en maladies du sang
Posologies : 2,5 mg/kg administrés par perfusion intraveineuse une fois toutes les 3 semaines. Il est recommandé de poursuivre le traitement jusqu’à progression de la maladie ou l’apparition d’une toxicité inacceptable
Mécanisme d'action :
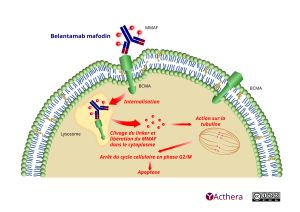
Le belantamab mafodotin se lie au BCMA à la surface de la cellule et est rapidement internalisé. Une fois dans la cellule tumorale, l’agent cytotoxique est libéré et perturbe le réseau de microtubules, ce qui entraîne l’arrêt du cycle cellulaire et l’apoptose. L’anticorps favorise le recrutement et l’activation des cellules effectrices immunitaires, tuant les cellules tumorales par cytotoxicité et phagocytose dépendantes de l’anticorps. L’apoptose induite par le belantamab mafodotin s’accompagne de marqueurs de mort cellulaire immunogène, qui peuvent favoriser une réponse immunitaire adaptative contre les cellules tumorales.
Au centre de l’image une cellule NK ou Lymphocyte, sur sa surface un belantamab mafodin (un anticorps humanisé I g G 4) muni d’un agent cytotoxique, le Monomethylastatin F (M M A F) figuré ici par 4 sphères.
Le belantamab mafodin se lie au récepteur BCMA présent à la surface de la cellule tumorale. Il est internalisé et enveloppé dans un lysosome qui va le digérer. Une flèche sort du lysosome et pointe sur les sphères de l’agent cytotoxique MMAF, elle est sous-titrée « Clivage du linker et libération du MMAF dans le cytoplasme »
À la droite du MMAF une flèche pointe vers « Action sur la tubuline ». Sous ce texte la tubuline et son réseau de microtubules sont perturbés. A gauche en descendant vers le centre de la cellule une flèche désigne le texte « Arrêt du cycle cellulaire en phase G2/M ». Sous ce texte une petite flèche pointe vers le texte « Apoptose ». L’apoptose est la conséquence de l’action de belantamab mafodin, qui dépose des marqueurs de mort cellulaire immunogène, qui peuvent favoriser une réponse adaptative immunitaire.
Le belantamab mafodin tue les cellules tumorales par cytotoxicité et phagocytose dépendantes de l’anticorps.
Effets indésirables les plus fréquents : Les effets indésirables les plus fréquents (≥ 30 %) étaient une kératopathie
(71 %) et une thrombopénie (38 %). Les effets indésirables graves les plus fréquemment rapportés étaient : pneumonie (7 %), fièvre (7 %) et réactions liées à la perfusion (3 %) (se référer au RCP pour avoir la liste complète des effets indésirables).
Contre-indications : Hypersensibilité à la substance active ou à l’un des excipients
Principales références :
- Ray U, Orlowski RZ. Antibody-Drug Conjugates for Multiple Myeloma: Just the Beginning, or the Beginning of the End? Pharmaceuticals (Basel). 2023 Apr 14;16(4):590. doi: 10.3390/ph16040590. PMID: 37111346; PMCID: PMC10145905
- Leong S, Lam HPJ, Kirkham Z, Popat R. Antibody drug conjugates for the treatment of multiple myeloma. Am J Hematol. 2023 Mar;98 Suppl 2:S22-S34. doi: 10.1002/ajh.26750. Epub 2022 Oct 24. PMID: 36199262
- Martino EA, Bruzzese A, Iaccino E, Labanca C, Mendicino F, Mimmi S, Lucia E, Olivito V, Neri A, Morabito F, Vigna E, Gentile M. Belantamab mafodotin in multiple myeloma. Expert Opin Biol Ther. 2023 May 27:1-5. doi: 10.1080/14712598.2023.2218543. Epub ahead of print. PMID: 37227998
- Talbot A, Bobin A, Tabone L, Lambert J, Boccaccio C, Deal C, Petillon MO, Allangba O, Agape P, Arnautou P, Belkhir R, Cailleres S, Chaoui D, Chrétien ML, Decaux O, Schulmann S, Frenzel L, Gastaud L, Huart A, Hulin C, Karlin L, Laribi K, Le Calloch R, Lenain P, Macro M, Manier S, Montes L, Moreau S, Moreau P, Morel V, Norwood J, Piocelle FO, Perrot A, Pica GM, Rey P, Schmitt A, Stoppa AM, Tiab M, Touzeau C, Vidal V, Vignon M, Vincent L, Van De Wyngaert Z, Zarnitsky C, Kerbouche N, Paka P, Leleu X, Arnulf B, Avet-Loiseau H; IFM: Intergroupe Francophone du Myélome. Real-world study of the efficacy and safety of belantamab mafodotin (GSK2857916) in relapsed or refractory multiple myeloma based on data from the nominative ATU in France: IFM 2020-04 study. Haematologica. 2023 Apr 20. doi: 10.3324/haematol.2022.281772. Epub ahead of print. PMID: 37078253
- Alegre A, Benzo G, Alonso R, Martínez-López J, Jimenez-Ubieto A, Cuéllar C, Askari E, Prieto E, Aláez C, Aguado B, Velasco A, Krsnik I, Bocanegra A, Llorente L, Muñoz-Linares C, Morales A, Giménez E, Iglesias R, Martínez-Chamorro C, Alonso A, Jiménez-Montes C, Blanchard MJ; Grupo GM-GM. Real-World Outcomes of Belantamab Mafodotin for Relapsed/Refractory Multiple Myeloma (RRMM): Preliminary Results of a Spanish Expanded Access Program (EAP). Oncol Ther. 2023 Mar;11(1):83-96. doi: 10.1007/s40487-022-00212-5. Epub 2022 Dec 12. PMID: 36509945; PMCID: PMC9744371
- Lonial S, Lee HC, Badros A, Trudel S, Nooka AK, Chari A, Abdallah AO, Callander N, Sborov D, Suvannasankha A, Weisel K, Voorhees PM, Womersley L, Baron J, Piontek T, Lewis E, Opalinska J, Gupta I, Cohen AD. Longer term outcomes with single-agent belantamab mafodotin in patients with relapsed or refractory multiple myeloma: 13-month follow-up from the pivotal DREAMM-2 study. Cancer. 2021 Nov 15;127(22):4198-4212. doi: 10.1002/cncr.33809. Epub 2021 Jul 27. PMID: 34314018; PMCID: PMC8597112.
Liens :
- Human medicine European public assessment report (EPAR)
- HAS
- Base de données publique des médicaments
- ANSM
- Meddispar (pas de données au 5 juin 2023)
- Centre de référence sur les agents tératogènes (CRAT) (pas de données au 5 juin 2023)
Remarque :
Création de la fiche : Pr C. Carnoy
Dernière mise à jour : 5 juin 2023
Relecture par :