Tocilizumab (ROACTEMRA®)
Autre nom commercial : Actemra (USA)
Structure : AcM humanisé, IgG1k
Code ATC : L04AC07
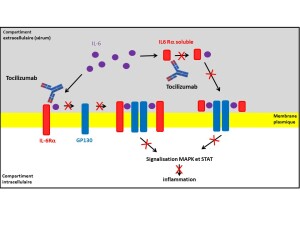
Cible: IL-6R ; récepteurs solubles et membranaires de l'IL-6
Mode de production : cellules d'ovaire de hamster chinois (CHO) par technique de l'ADN recombinant
Forme galénique : Flacon contenant soit 80 mg de tocilizumab dans 4 mL, soit 200 mg de tocilizumab dans 10 mL, soit 400 mg de tocilizumab dans 20 mL. Chaque mL de solution à diluer contient 20 mg de tocilizumab.
Mode d'administration : IV. Il existe une forme SC.
Date d'AMM : EMA 2009-2011 / FDA 2010-2011
Laboratoire : Roche / Chugai
Indications : Polyarthrite rhumatoïde, arthrite juvénile idiopathique (AJI)
Prix indicatif : 824,62 € pour 162 mg de tocilizumab
Usage : réservé à l'usage hospitalier
Posologies : Pour la polyarthrite rhumatoïde, la posologie recommandée est de 8 mg/kg administrée une fois toutes les 4 semaines. La posologie recommandée pour l'arthrite juvénile idiopathique (AJI) est de 8 mg/kg toutes les 2 semaines chez les patients dont le poids est supérieur ou égal à 30 kg ou de 12 mg/kg toutes les 2 semaines chez les patients pesant moins de 30 kg.
Mécanisme d'action :
Effets indésirables les plus fréquents: infection respiratoire
Contre-indications : hypersensibilité au médicament, patient avec infection sévère
Principales références :
- Fiche de l'Association Nationale de Défense contre l'Arthrite Rhumatoide (ANDAR) : ROACTEMRA® [pdf][1]
- Avis de la HAS sur Roactemra
- Lien vers Human medicine European public assessment report (EPAR)
- Lien vers la fiche info de la base de données publique des médicaments
- IMGT
- HeTOP
Remarque :
Dernière mise à jour : Novembre 2021
Relecture par : Dr Emmanuel Hermann