Palivizumab (SYNAGIS®)
Structure : AcM humanisé, IgG1k
Code ATC : J06BB16
Nomenclature Ge : IgG1κ G1e0
Cible: Site antigénique A de la glycoprotéine F du virus respiratoire syncytial (VRS)
Mode de production : produit par la technologie de l'ADN recombinant sur des cellules hôtes de myélome de souris
Forme galénique : Flacons à usage unique de 0,5 ml et de 1 ml à 100 mg / ml
Mode d'administration : IM dans la cuisse
Date de la première AMM : FDA 1998 / EMA 1999
Laboratoires : Arexis AB / Astrazenaca
Indications : prévention des infections respiratoires graves, dues au virus respiratoire syncytial (VRS) nécessitant une hospitalisation chez les enfants à risque élevé d'infection à VRS :
Enfants nés à 35 semaines d'âge gestationnel ou moins et de moins de 6 mois au début de l'épidémie saisonnière à VRS.
Enfants de moins de 2 ans ayant nécessité un traitement pour dysplasie bronchopulmonaire au cours des 6 derniers mois.
Enfants de moins de 2 ans atteints d'une cardiopathie congénitale avec retentissement hémodynamique.
Prix indicatif 2023 : 403,436 euros le flacon de 0,5 ml ; 669,926 euros le flacon de 1 ml (idem 2021)
Posologies : La posologie recommandée de 15 mg/kg, administrés une fois par mois pendant les périodes à risque d'infections communautaires à VRS. Le volume (exprimé en ml) de palivizumab à administrer à des intervalles d'un mois = [poids du patient en kg] multiplié par 0,15. Lorsque cela est possible, la première dose doit être administrée avant le début de la saison de l'épidémie à VRS et les doses suivantes, chaque mois pendant toute la durée de cette saison.
Mécanisme d'action :
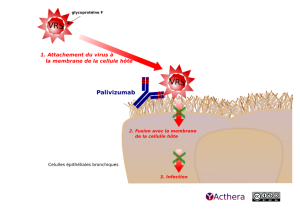
Il y a deux principales protéines immunogènes à la surface du virus respiratoire syncytial: la glycoprotéine F (fusion) et G (facteur d'attachement à l'épithélium bronchique). La protéine F est hautement conservée et nécessaire pour infecter les cellules alors que la protéine G est variable. Le virus s'adsorbe à la surface des cellules, via la protéine G et la protéine F (fusion entre membranes du virus et de la cellule hôte). Le palivizumab bloque l'entrée du virus en liant la protéine F du VRS, ce qui empêche la fusion des membranes et la formation de syncitia (qui permet au virus de passer de cellules en cellules).
Effets indésirables les plus fréquents: fièvre, éruption cutanée et réaction au site d'injection ; infections cutanées (se référer au RCP pour avoir la liste complète des effets indésirables)
Contre-indications : hypersensibilité à la substance active ou à l'un des excipients
Principales références :
- Fitzpatrick T, McNally JD, Stukel TA, Kwong JC, Wilton AS, Fisman D, Guttmann A. Palivizumab's real-world effectiveness: a population-based study in Ontario, Canada, 1993-2017. Arch Dis Child. 2021 Feb;106(2):173-179. doi: 10.1136/archdischild-2020-319472. Epub 2020 Aug 28. PMID: 32859612; PMCID: PMC7841493.
- Papenburg J, Defoy I, Massé E, Caouette G, Lebel MH. Impact of the Withdrawal of Palivizumab Immunoprophylaxis on the Incidence of Respiratory Syncytial Virus (RSV) Hospitalizations Among Infants Born at 33 to 35 Weeks' Gestational Age in the Province of Quebec, Canada: The RSV-Quebec Study. J Pediatric Infect Dis Soc. 2021 Apr 3;10(3):237-244. doi: 10.1093/jpids/piaa046. PMID: 32530035; PMCID: PMC8023310.
- Luna MS, Manzoni P, Paes B, Baraldi E, Cossey V, Kugelman A, Chawla R, Dotta A, Rodríguez Fernández R, Resch B, Carbonell-Estrany X. Expert consensus on palivizumab use for respiratory syncytial virus in developed countries. Paediatr Respir Rev. 2020 Feb;33:35-44. doi: 10.1016/j.prrv.2018.12.001. Epub 2018 Dec 18. PMID: 31060948.
- Drugs and Lactation Database (LactMed) [Internet]. Bethesda (MD): National Library of Medicine (US); 2006–. Palivizumab. 2021 Apr 19. PMID: 29999653.
Liens :
- Avis de la HAS sur Synagis
- Lien vers Human medicine European public assessment report (EPAR)
- Base de données publique des médicaments
- IMGT
Remarque :
Dernière mise à jour : 27/07/2021
Relecture par : Dr P. De Nadaï