Obinutuzumab (GAZYVARO®)
Autre nom : afutuzumab
Structure : AcM humanisé, IgG1k
Code ATC : L01XC15 ou L01FA03
Nomenclature Ge : IgG1κ G1e5
Cible: CD20
Mode de production : Produit dans les cellules ovariennes de hamster chinois par la technologie de l’ADN recombinant.
Forme galénique : Solution à diluer pour perfusion (1000 mg pour 40 mL soit 25 mg/mL).
Mode d'administration : IV
Conservation :
Le flacon se conserve fermé 3 ans au réfrigérateur entre 2 et 8°C.
Après dilution, la stabilité physico-chimique a été démontrée dans une solution injectable de chlorure de sodium 9 mg/ml (0,9 %) à des concentrations de 0,4 mg/ml à 20 mg/ml pendant 24 heures à une température comprise entre 2 °C et 8 °C et pendant 48 heures supplémentaires (y compris le temps de perfusion) à une température ≤ 30 °C.
Sur le plan microbiologique, la solution diluée pour perfusion doit être utilisée immédiatement. Si elle n'est pas utilisée immédiatement, les durées et les conditions de conservation jusqu'à l'emploi sont sous la responsabilité de l'utilisateur et ne doivent normalement pas dépasser 24 heures entre 2 °C et 8 °C, à moins que la dilution n'ait été réalisée dans des conditions d'asepsie contrôlées et validées.
Date de la première AMM : FDA 2013- EMA 2014
Laboratoires : Roche pharma
Indications :
- Leucémie lymphoïde chronique (LLC) : en association au chlorambucil pour le traitement des patients non précédemment traités, et présentant des comorbidités les rendant inéligibles à un traitement à base de fludarabine à pleine dose.
- Lymphome folliculaire (LF) :
Associé à une chimiothérapie en induction, suivi d'un traitement d'entretien par Gazyvaro chez les patients répondeurs atteints de lymphome folliculaire avancé non précédemment traités .
Associé à la bendamustine en induction, suivi d'un traitement d'entretien par Gazyvaro, chez les patients atteints de lymphome folliculaire (LF) en cas de non-réponse ou de progression, pendant ou dans les 6 mois suivant un traitement incluant du rituximab.
Prix indicatif : 2892,65 euros
Usage : Réservé à l'usage hospitalier. Prescription réservée aux spécialistes et services d’hématologie ou aux médecins compétents en maladie du sang.
Posologie : 1000 mg par jour aux jours 1, 2, 8, 15 du premier cycle, puis tous les premiers jours (J1) des cycles 2 à 6.
/!\ Les patients ayant une masse tumorale importante et/ou un nombre élevé de lymphocytes circulants (> 25 x 10G/L) et/ou une insuffisance rénale (ClCr < 70 ml/min) sont considérés à risque de syndrome de lyse tumorale et doivent recevoir un traitement prophylactique (hydratation appropriée + administration d’uricostatiques) 12 à 24h avant la perfusion de GAZYVARO®.
/!\ Une prémédication par corticoïdes, analgésiques et anti-histaminique est recommandée pour les patients atteints de LF et elle est obligatoire pour les patients atteints de LLC.
/!\ La suspension des traitements antihypertenseurs doit donc être envisagée 12 heures avant chaque perfusion de Gazyvaro, ainsi que pendant toute la durée de la perfusion et pendant la première heure suivant la fin de l'administration (réaction d'hypotension fréquente)
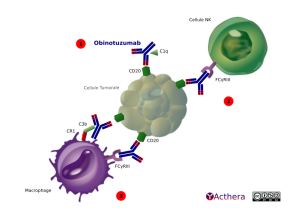
Mécanisme d'action :
L'obinutuzumab est un anticorps monoclonal modifié afin d'améliorer l'affinité de son Fc aux FcgR3 des cellules NK, des macrophages et des monocytes. Il est dirigé contre l'antigène CD20 retrouvé sur les lymphocytes pré-B et matures tumoraux et non tumoraux. En se liant au CD20 obinutuzumab est capable de provoquer la mort de ces lymphocytes, mais également de recruter par un mécanisme d'ADCC des cellules effectrices reconnaissant le FcgR3. Ainsi, ces cellules vont lyser les cellules tumorales. Cet anticorps est également capable de recruter les protéines du complément mais ce mécanisme n'est pas majeur
Effets indésirables les plus fréquents : infections, diarrhées, vomissements, fièvre, anémie, neutropénie, thrombocytopénie, syndrome de lyse tumorale, hyperuricémie, insomnies, céphalées, toux, alopécie, prurit, arthralgie et douleurs des extrémités...
Contre-indications : hypersensibilité au médicament
Utilisation chez la femme enceinte : Les femmes en âge de procréer doivent utiliser une contraception efficace pendant le traitement par Gazyvaro et jusqu'à 18 mois après son arrêt. Une étude sur la reproduction conduite chez le singe Cynomolgus n'a pas révélé d'effet embryofoetotoxique ni tératogène, mais a entraîné une déplétion complète en lymphocytes B dans la descendance ; chez celle-ci, les numérations des lymphocytes B se sont normalisées et la fonction immunitaire a été rétablie dans les 6 mois suivant la naissance. Il n’existe pas de données sur l’utilisation de l’obinutuzumab chez la femme enceinte. Gazyvaro ne doit pas être utilisé chez la femme enceinte sauf si le bénéfice attendu est supérieur au risque potentiel d’une telle utilisation. Il convient alors de reporter la vaccination par les vaccins vivants atténués pour le nourrisson.
Principales références :
- Goede et al., 2014 ; Golay J et al. 2013 ; Lee et al., 2014
Liens :
- Avis de la HAS sur Gazyvaro
- Lien vers Human medicine European public assessment report (EPAR)
- Lien vers la monographie de la FDA
- IMGT/DB
- Meddispar - pas de données au 30 mars 2023
- CRAT - pas de données au 30 mars 2023
- Vidal
Remarque :
Dernière mise à jour : Mars 2023
Par : Mathilde GLAZIOU