Fremanezumab (AJOVY®)
Autre nom : Fremanezumab-vfrm
Structure : IgG2a/kappa humanisé
Code ATC : N02CD03
Nomenclature Ge : IgG1κ G2e1
Cible: Calcitonin Gene-Related Peptide (CGRP)
Forme galénique : Seringue préremplie ou stylo contenant 225 mg de frémanezumab
Mode d'administration : SC
Conservation : Le médicament se conserve au réfrigérateur entre 2 et 8°C. Il est préférable de sortir le médicament 30 min avant injection. Le médicament peut se conserver à température ambiante maximum pendant 7 jours.
Date de la première AMM : EMA mars 2019 / FDA septembre 2018
Laboratoires : Teva
Indications : Prophylaxie de la migraine chez l'adulte présentant au moins 4 jours de migraine par mois
Prix indicatif : XXX
Usage : prescription (initiale et renouvellement) réservée aux spécialistes en neurologie. Durée maximale de prescription de 1 an.
Posologies : 1 injection de 225 mg une fois par mois (administration mensuelle) ou 3 injections à la suite (675 mg) tous les trois mois (administration trimestrielle)
Mécanisme d'action :
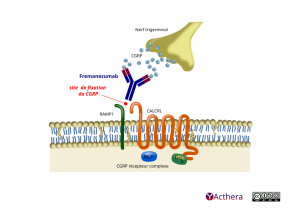
Le frémanezumab se lie de manière sélective au Calcitonin Gene-Related Peptide (CGRP) et empêche les deux isoformes du CGRP (α- et ß-CGRP) de se lier au récepteur du CGRP. Le mécanisme d'action précis par lequel le frémanezumab prévient les crises de migraine n'est pas connu, mais l'on pense que son effet modulateur au niveau du ganglion trigéminal permet de prévenir la migraine. Il a été montré que les taux de CGRP augmentent de manière significative pendant la crise de migraine et qu'ils reviennent ensuite à la normale avec le soulagement des céphalées.
Le nerf trigerminal – évoquant un parapluie inversé – est au-dessus d’une cellule, il expulse des molécules CGRP (peptide relié au gène de la calcitonine). La peptide contribue à l’inflammation et à la vasodilatation associée à la crise de migraine.
Le fremanezumab (A c M humanisé I g G 1) cible les formes alpha et bêta du CGRP dès leur sortie du nerf trigerminal, avant que celles-ci ne se lient au CGRP comprenant plusieurs éléments. Il se compose de deux protéines cytoplasmisques ; RAMP1 coudé au-dessus de la cellule, qui traverse la membrane et se termine dans le cytoplasme, et de CALCRL qui ondule ayant trois boucles extracellulaires et trois boucles intracellulaires, en dessous, deux protéines cytoplasmique RCP, une dernière boucle intracellulaire de CALCRL se lie à la sous unité alpha de la protéine GS.
Les molécules CGRP ne peuvent se lier au récepteur CGRP. En interceptant ces molécules de peptides le fremanezumab fait baisser significativement l’intensité de la crise.
Effets indésirables les plus fréquents:
Très fréquent : Douleur,induration, érythème au site d'injection.
Fréquent : prurit au site d'injection
Contre-indications : Hypersensibilité à la substance active ou à l'un des excipients
Principales références :
- Hoy SM. Fremanezumab: First Global Approval [published correction appears in Drugs. 2019 Apr;79(5):585]. Drugs. 2018;78(17):1829–1834. doi:10.1007/s40265-018-1004-5
- Silberstein SD, Dodick DW, Bigal ME, et al. Fremanezumab for the Preventive Treatment of Chronic Migraine. N Engl J Med. 2017;377(22):2113–2122. doi:10.1056/NEJMoa1709038
Liens :
- Human medicine European public assessment report (EPAR)
- HAS
- Base de données publique des médicaments
- ANSM (pas disponible au 1er juin 2022)
- Meddispar (pas disponible au 1er juin 2022)
- Centre de référence sur les agents tératogènes (CRAT) (pas disponible au 1er juin 2022)
- HeTOP[2]
Note :
Dernière mise à jour : 1er juin 2022
Relecture par : Pr C. Carnoy