Belatacept (NULOJIX®)
Structure : protéine de fusion soluble constituée du domaine extracellulaire modifié de l'antigène 4 cytotoxique humain associé au lymphocyte T (CTLA 4) lié à la partie Fc (domaines charnière-CH2-CH3) d'une immunoglobuline G1 humaine (IgG1)
Code ATC : L04AA28
Cible: CD80/CD86
Forme galénique : Flacon contenant 250 mg de bélatacept à reconstituer pour obtenir un solution à 25 mg/ml de bélatacept.
Mode d'administration : IV
Date de la première AMM : FDA 2011 / EMA 2011
Laboratoires et lien vers Nulojix: Bristol-Myers Squibb
Indications : en association aux corticoïdes et à l'acide mycophénolique pour éviter le rejet du greffon chez les adultes recevant une transplantation rénale
Prix indicatif (2021) : 391 euros HT (NULOJIX 250MG PERF FL+SRG ) = prix de cession aux établissements de santé (Journal officiel)
Usage : réservé à l'usage hospitalier
Posologies :
- phase initiale : jour de la transplantation J1 (avant l'implantation) 10 mg/kg puis 10 mg/kg à J5, 14, 28 puis fin des semaines 8 et 12 après la transplantation
- phase d'entretien : 5 mg/kg toutes les 4 semaines (± 3 jours), à partir de la fin de la semaine 16 après la transplantation
Pour les patients mis sous traitement par NULOJIX au moment de la transplantation (« patients nouvellement transplantés »), il est recommandé d'ajouter un antagoniste du récepteur de l'interleukine-2 (IL-2)
Mécanisme d'action :
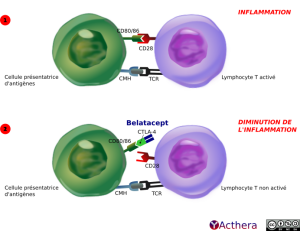
Belatacept se lie à CD80 (B7.1) et CD86 (B7.2) à la surface des cellules présentatrices de l'antigène, bloquant la costimulation des lymphocytes T via CD28. La protéine de fusion belatacept inhibe l'activation des LcT cytotoxiques, responsables du rejet de la greffe de rein.
En haut schéma 1, intitulé INFLAMMATION. À gauche une cellule porte la mention « cellule présentatrice d'antigènes (ou C P A) » interagit un lymphocyte T légendé « Lymphocyte T activé » à sa droite. Sur la surface de la C P A, le ligand CD80 86, qui se lie au récepteur CD28 du lymphocyte T. Plus bas, à la surface de la C P A, le récepteur CMH tenant l’Ag (antigène) est en contact avec le TCR présent à la surface du lymphocyte T. Le lymphocyte T est activé par ces deux signaux de stimulation
En bas schéma 2, intitulé "DIMINUTION DE L'INFLAMMATION", à gauche une CPA à sa droite un lymphocyte T. Le belatacept (une protéine de fusion Fc modifiée de I g G 1 humaine) associée au CTL A 4 (antigène 4 cytotoxique humain) cible le récepteur CD 80 86, présent sur la C P A via CTL A 4. Plus bas à la surface de la C P A, le récepteur C M H tenant l’Ag, est en contact avec le T C R du lymphocyte T. Le belatacept empêche que le CD28 déclenche la co-stimulation nécessaire, l’activation du lymphocyte T n’a pas lieu, il inhibe les lymphocytes cytotoxiques, responsables du rejet de la greffe de rein.
Effets indésirables les plus fréquents: infections urinaires, infections à cytomégalovirus, neutropénie, leucopénie, céphalées (se référer au RCP pour avoir la liste complète des effets indésirables)
Contre-indications : hypersensibilité au médicament ou à l'un des excipients, patients transplantés séronégatifs (ou de statut sérologique inconnu) pour le virus Epstein Barr
Principales références :
- Noble J, Jouve T, Janbon B, Rostaing L, Malvezzi P. Belatacept in kidney transplantation and its limitations. Expert Rev Clin Immunol. 2019 Apr;15(4):359-367. doi: 10.1080/1744666X.2019.1574570. Epub 2019 Feb 7. PMID: 30676815.
- Drugs and Lactation Database (LactMed) [Internet]. Bethesda (MD): National Library of Medicine (US); 2006–. Belatacept. 2021 Jun 21. PMID: 29999697.
- Schwarz C, Mahr B, Muckenhuber M, Wekerle T. Belatacept/CTLA4Ig: an update and critical appraisal of preclinical and clinical results. Expert Rev Clin Immunol. 2018 Jul;14(7):583-592. doi: 10.1080/1744666X.2018.1485489. Epub 2018 Jun 25. PMID: 29874474.
- Perez CP, Patel N, Mardis CR, Meadows HB, Taber DJ, Pilch NA. Belatacept in Solid Organ Transplant: Review of Current Literature Across Transplant Types. Transplantation. 2018 Sep;102(9):1440-1452. doi: 10.1097/TP.0000000000002291. PMID: 29787522.
- Chopra B, Sureshkumar KK. Co-stimulatory blockade with belatacept in kidney transplantation. Expert Opin Biol Ther. 2014 May;14(5):563-7. doi: 10.1517/14712598.2014.896332. Epub 2014 Mar 12. PMID: 24620724.
Liens :
- Human medicine European public assessment report (EPAR)
- avis de la HAS sur Nulojix
- Base de données publique des médicaments
- ANSM. Le site détaille les modalités pratiques d'administration et propose une fiche d'information patient
Remarque :
Dernière mise à jour : janvier 2022
Relecture par : Pr C. Carnoy