Adalimumab (HALIMATOZ®)
• Structure : AcM humain, IgG1k
• Cible: TNF (tumor necrosis factor) soluble et membranaire
• Mode d'administration : SC
• Date d'AMM : FDA XXX / EMA juillet 2018
• Laboratoires : Sandoz GmbH
• Indications : polyarthrite rhumatoïde, arthrite juvénile idiopathique, spondylarthrite axiale, rhumatisme psoriasique, psoriasis, hidrosadénite suppurée, uvéite
• Prix indicatif : xxx
• Usage : prescription initiale hospitalière annuelle
• Posologies :
Pour la polyarthrite, la spondylarthrite ankylosante, le rhumatisme psoriasique et l'arthrite juvénile idiopathique 40 mg/2 semaines.
Pour le psoriasis et l'uvéite 80 mg d'emblée puis 40 mg/2 semaines dès la semaine 1.
Pour l'hidrosadénite suppurée (HS) une dose initiale de 160 mg au Jour 1 (administrée sous forme de 4 injections de 40 mg sur un jour ou de 2 injections de 40 mg par jour pendant deux jours consécutifs), suivie d'une dose de 80 mg deux semaines après au Jour 15 (administrée sous forme de 2 injections de 40 mg sur un jour). Deux semaines plus tard (Jour 29), poursuivre avec une dose de 40 mg chaque semaine ou de 80 mg toutes les deux semaines (administrés sous forme de deux injections de 40 mg par jour).
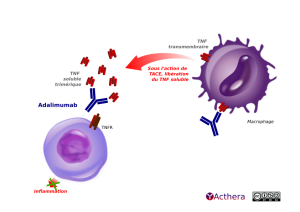
• Mécanisme d'action :
L'adalimumab bloque le TNF trimérique soluble et membranaire, ce qui empêche l'interaction avec les récepteurs p55 (TNFR1) et p75 (TNFR2) situés à la surface cellulaire, qui aurait permis l'activation de la voie NF-kB avec synthèse de cytokines pro-inflammatoires. La cascade inflammatoire est ainsi bloquée : diminution de l'expression de molécules d'adhésion diminuant ainsi le processus de diapédèse, et de recrutements de macrophages, lymphocytes et neutrophiles.
•
Effets indésirables les plus fréquents:
Contre-indications :
Principales références :
Principales références :
- fiche médicament du adalimumab sur le site du GETAID
- Lien vers Human medicine European public assessment report (EPAR)